
Các triệu chứng và cách điều trị bệnh sốt xuất huyết Dengue
Sốt xuất huyết (hay còn gọi là Dengue) là bệnh do 4 loại virus sốt xuất huyết gây ra. Các virus này là những virus gây ra tình trạng nhiễm trùng ở phía Tây của sông Nile và tình trạng sốt vàng da.
Sốt xuất huyết dengue.
Ước tính trên thế giới mỗi năm có khoảng 96 triệu ca nhiễm bệnh trên toàn thế giới. Hầu hết các trường hợp này thường xảy ra ở khu vực nhiệt đới do điều kiện thuận lợi để phát triển 4 loại virus gây bệnh.
Các nước có nhiều nguy cơ xảy ra tình trạng sốt xuất huyết là:
Ấn Độ
Đông Nam Á
Miền Nam Trung Quốc
Đài Loan
Các đảo Thái Bình Dương
Các quốc gia vùng Caribe (trừ Cuba và quần đảo Cayman)
Mexico
Châu phi
Trung và Nam Mỹ (trừ Chile, Paraguay và Argentina)
Virus sốt xuất huyết thường nhiễm vào cơ thể thông quan các vết cắn của muỗi Aedes. Những con muỗi này chứa virus dengue và khi cắn sẽ truyền nhiễm cho chúng ta và bệnh sốt xuất huyết không có khả năng truyền nhiễm từ người sang người.
Các triệu chứng của sốt xuất huyết
Các triệu chứng của sốt xuất huyết thường bắt đầu sau 4-6 ngày sau khi nhiễm và kéo dài tới 10 ngày. Các triệu chứng bao gồm:
Sốt cao đột ngột.
Nhức đầu nặng
Đau phía sau mắt
Đau cơ và khớp
Mệt mỏi
Buồn nôn
Nôn
Phát ban da, xuất hiện từ 2-5 ngày sau khi khởi phát sốt
Chảy máu nhẹ (như chảy máu mũi, chảy máu nướu răng, hoặc dễ bị bầm tím)
Và đôi khi các triệu chứng trên khi nhẹ dễ nhầm lẫn với tình trạng ốm thông thường mà mọi người hay gặp nên không được để ý lắm. Tuy nhiên nếu không được điều trị kịp thời có thể các triệu chứng tiền triển dẫn đến xuất huyết ồ ạt, shock và tử vong (Hội chứng shock Dengue - DSS) đặc biệt là trẻ em.
Những người có hệ miễn dịch yếu hoặc tái phát sốt xuất huyết lần 2 trở đi được cho là nguy cơ cao hơn bị xuất huyết.
Chẩn đoán sốt xuất huyết:
Để có thể chẩn đoán xác định bệnh sốt xuất huyết thì các bác sĩ cũng như nhân viên y tế cần phải xét nghiệm xác định virus và các kháng thể đối với nó. Và nếu bạn bị phát bệnh sau khi du lịch hoặc di chuyển qua vùng nhiệt đới thì nên nói cho bác sĩ để họ dễ dàng hơn trong việc chẩn đoán bệnh.
Điều trị sốt xuất huyết
Không có thuốc đặc trị bệnh sốt xuất huyết. Và chúng ta chỉ có thể điều trị triệu chứng của bệnh:
Sử dụng Paracetamol để giảm đau hạ sốt cho bệnh nhân. Tuyệt đối không dùng aspirin do có thể làm tăng nguy cơ xuất huyết.
Nghỉ ngơi uống nhiều nước.
Ngăn chặn sốt xuất huyết
Không có thuốc chủng ngừa bệnh sốt xuất huyết. Cách tốt nhất để ngăn ngừa căn bệnh này là ngăn chặn muỗi bị nhiễm bệnh cắn, đặc biệt là nếu bạn đang sống hoặc đi du lịch tới một khu vực nhiệt đới bằng cách:
Tránh xa khu vực dân cư đông dân cư nếu có thể.
Sử dụng thuốc chống muỗi, ngay cả trong nhà.
Khi ở ngoài trời, mặc áo sơ mi dài tay và quần dài.
Khi ở trong nhà, sử dụng điều hòa không khí nếu có.
Nếu khu vực ngủ không được sàng lọc hoặc máy lạnh, sử dụng màn chống muỗi.
Nếu bạn có những triệu chứng của bệnh sốt xuất huyết hãy đi khám ngay lập tức.
Thường xuyên tìm và vệ sinh quanh nhà với những nơi tụ nước dễ là nơi muỗi sinh sản.
Nếu trong nhà bị sốt xuất huyết báo ngay cơ quan y tế để có thể đến để tìm và ngăn chặn ổ bệnh khỏi bị phát dịch.
Cách lựa chọn phương pháp hóa trị liệu bệnh ung thư phù hợp từng giai đoạn bệnh
Hoá trị liệu ung thư
1. Giới thiệu về hóa trị liệu ung thư:
Hoá trị liệu ung thư.
Hoá trị ung thư là phép điều trị ung thư sử dụng các thuốc chống ung thư. Những thuốc này thường được dùng như là một phần của đa trị liệu, cùng với phẫu thuật và/hoặc xạ trị nhằm đạt được và duy trì sự lui bệnh. Quá trình điều trị này thường lâu dài, các thuốc được sử dụng đơn độc hay kết hợp vào giữa các đợt tấn công hay trong chu trình điều trị, và phần lớn phụ thuộc vào loại và đặc điểm của khối u.
Việc giám sát bệnh nhân diễn ra trong suốt quá trình điều trị nhằm ghi nhận đáp ứng điều trị hoặc diễn tiến của bệnh, và mục tiêu điều trị theo đó được điều chỉnh cho phù hợp.
Theo truyền thống, hoá trị ung thư thực hiện theo các hướng dẫn điều trị được đưa ra bởi các chuyên khoa lâm sàng phù hợp, chẳng hạn, các tiêu chuẩn chẩn đoán, điều trị và theo dõi được đưa ra bởi Hiệp hội Ung bướu Châu Âu (ESMO- European Society for Medical Oncology). Tuy nhiên, hiện nay người ta nhận thấy các khối u không đồng nhất giữa các bệnh nhân và trên cùng một bệnh nhân, cho nên nỗ lực cá nhân hoá điều trị theo đặc điểm khối u và bệnh nhân đang được nghiên cứu và đưa vào thực hành. Sinh học phân tử và các kĩ thuật chẩn đoán như chụp cộng hưởng từ (MRI), và chụp cắt lớp phát xạ (PET) đã cho thấy một loạt các dấu ấn sinh học có thể dùng như các chỉ số tiên lượng. Các chỉ số tiên lượng, chỉ số giúp dự đoán sự sống của bệnh nhân sau một đặc trị, có giá trị nhất định trong việc lựa chọn công thức điều trị cho bệnh nhân bao gồm cả các điều trị chuẩn và các thuốc chống ung thư mới trong các thử nghiệm lâm sàng. Chúng cũng giúp xác định sự cần thiết phối hợp thêm các điều trị khác như xạ trị.
2. Thời điểm của hoá trị liệu:
Mục đích của hoá trị liệu là đem lại sự lui bệnh, tức là, loại trừ hoàn toàn bệnh trong ít nhất 1 tháng. Thách thức của trị liệu ung thư là ngăn chặn sự tái phát có thể xảy ra ở tại chỗ hoặc ở khoảng cách xa (di căn) so với khối u nguyên phát. Để giải quyết vấn đề này, các chiến lược bổ sung được áp dụng trước hoặc theo sau đợt lui bệnh.
Vì vậy, hoá trị liệu được phân loại theo thời điểm như sau:
Hoá trị cảm ứng (Induction chemotherapy): là phép điều trị khởi đầu nhằm mục đích làm giảm tế bào ung thư đáng kể, và lý tưởng là đạt được lui bệnh hoàn toàn. Kết quả của hoá trị cảm ứng có thể là 1 đáp ứng hoàn toàn- bệnh biến mất trong 1 tháng; đáp ứng 1 phần- thể tích khối u giảm 50% hoặc hơn; bệnh ổn định – thể tích khối u giảm dưới 50% và không phát sinh ở vị trí mới trong vòng ít nhất 1 tháng; hoặc bệnh tiến triển – thể tích khối u tăng 25% hoặc hơn, hoặc có bằng chứng bệnh phát sinh ở vị trí mới.
Hoá trị củng cố/ tăng cường (consolidation/ intensification chemotherapy): Quản lý sự lui bệnh sau đợt lui bệnh ban đầu để kéo dài thời gian không có bệnh và thời gian sống. Trong khi hoá trị củng cố sử dụng cùng các thuốc như bước hoá trị cảm ứng tạo được sự lui bệnh, liệu pháp tăng cường sử dụng các thuốc không đề kháng chéo với hoá trị cảm ứng.
Hoá trị bổ trợ (adjuvant chemotherapy): được đưa ra tiếp theo điều trị tại chỗ như phẫu thuật hoặc xạ trị, được dùng để điều trị bệnh ở mức độ vi thể và ngăn ngừa tái phát tại chỗ.
Hoá trị tân bổ trợ (neoadjuvant chemotherapy): được đưa ra trước khi điều trị tại chỗ nhằm nâng cao hiệu quả điều trị, chẳng hạn làm nhỏ khối u trước phẫu thuật.
Hoá trị duy trì (maintenance chemotherapy): hoá trị với liều thấp, kéo dài được thực hiện trên các bệnh nhân ngoại trú hoặc ngoài cộng đồng để kéo dài thời gian lui bệnh và đạt được mục tiêu điều trị.
3. Các giai đoạn của ung thư nên được điều trị như thế nào?
Để xác định giai đoạn ưng thư chúng ta dựa trên kết quả cận lâm sàng như:
X-quang ngực / CT Scan/ MRI não để phát hiện di căn não nếu có.
Sinh thiết hạch.
PET, xạ hình xương để phát hiện di căn xương.
Lựa chọn phương pháp hóa trị liệu phù hợp với từng giai đoạn ung thư:
Giai đoạn 1-2: Phẫu thuật cộng với hoá trị bổ trợ và /hoặc hóa trị tân bổ trợ. Đối với các khối u không thể phẫu thuật: xạ trị điều trị.
Giai đoạn 3: Cảm ứng hóa trị liệu cộng với phẫu thuật cắt bỏ. Đối với các khối u không thể phẫu thuật, hóa trị với các thuốc chứa Platinum (như cisplatin) cộng với xạ trị lồng ngực.
Giai đoạn 4: Hóa trị phối hợp các thuốc chứa Platinum kéo dài sự sống, cải thiện chất lượng cuộc sống và kiểm soát các triệu chứng.
Đánh giá đáp ứng: Bắt buộc sau hai hoặc ba chu kỳ hóa trị sau khi lặp lại xét nghiệm chẩn đoán hình ảnh.
Theo dõi: Tiền sử và khám thực thể mỗi 4 tháng trong 2 năm đầu và mỗi 6 tháng cho các năm tiếp theo.
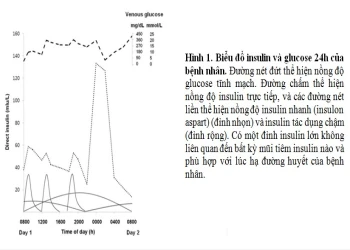
Case hạ glucose máu về đêm tái phát ở một bệnh nhân đái tháo đường type 1
CA LÂM SÀNG
Một bệnh nhân nam 39 tuổi mắc Đái tháo đường(ĐTĐ) type 1 được nhập viện kèm nhiễm toan ceton nặng và nhiễm trùng đường hô hấp trên. Các xét nghiệm sinh hóa lúc nhập viện: Glucose huyết tương tĩnh mạch 933 mg/dl (51.8 mmol/L) (giới hạn bình thường: 72 – 140 mg/dl hoặc 4.0 – 7.8 mmol/L), bicarbonate: 14.7 mmol/L (22 – 31 mmol/L), β – hydroxybutyrate > 6 mmol/L (< 0.6 mmol/L) và pH động mạch 7.28 (7.35 – 7.45). Bệnh nhân được chữa trị bằng truyền dịch tĩnh mạch và truyền Insulin tĩnh mạch quãng ngắn, và bệnh nhân phục hồi nhanh.
Bệnh nhân đã được chẩn đoán tiểu đường type 1 năm 33tuổi khi có biểu hiện cơn nhiễm toan ceton. Kháng thể Glutamic acid decarboxylate tăng tại thời điểm chẩn đoán 10.6 U/mL (giá trị bình thường < 1 U/mL) và nồng độ peptide C sau bữa ăn không phát hiện được. Việc kiểm soát glucose máu của bệnh nhân sau đó là kém, với HbA1c tăng trong khoảng 8.9% đến 15.6%, điều này dẫn đến các biến chứng về thần kinh ngoại vi và tự động như cơn đau thần kinh ngoại biên và rối loạn cương dương. Tiền sử bệnh nhân gồm có sa van tim, tăng huyết áp và rồi loạn lipid máu. BN được kê chế độ Insulin tiêm quãng ngắn nền (basal – bolus insulin) gồm: insulin tác dụng dài 2 lần/ngày (insulin detemir 10U trước bữa sáng và 7U trước bữa tối) phối hợp insulin tác dụng nhanh 3 lần/ngày (insulin aspart 5U trước bữa sáng và 3U trước bữa trưa và 4U trước bữa tối), simvastatin, sildenafil, pregabalin, và omeprazol. BN không dùng sulfonylurea và không dùng thức uống có cồn.
Sau khi xử lí nhiễm toan ceton, bệnh nhân được bắt đầu lại chế độ Insulin tiêm quãng ngắn nền như trước khi nhập viện. sau đó, chế độ insulin của bệnh nhân được điều chỉnh trong lần nhập viện này, và bệnh nhân thay đổi glucose máu trong khoảng rộng và bị hạ glucose máu tái phát về đêm. Điển hình, glucose máu tăng nghiêm trọng trong ngày (glucose mao mạch: 205- 553 mg/dl hay 11.4 – 30.7 mmol/L) nhất là sau bữa ăn. Trong khi các biểu hiện hạ glucose máu xảy ra liên tục lúc 24h – 2h30 hàng đêm (glucose máu mao mạch: 34 – 58 mg/dl hay 1.9 – 3.2 mmol/L) đi cùng với các triệu chứng đáp ứng giao cảm như toát mồ hôi, đánh trống ngực, căng thẳng
CÁC ĐIỂM CẦN XEM XÉT:
1. Những nguyên nhân gây hạ glucose máu tái phát ở bệnh nhân đang dùng liệu pháp insulin là gì?
2. Các phương pháp nào giúp chẩn đoán các nguyên nhân gây hạ glucose máu tái phát?
3. Kháng thể kháng insulin có thể gây ra hạ glucose máu không ?
Khám lâm sàng cho thấy các dấu hiệu sống ổn định và bệnh nhân gầy với chỉ số khối cơ thể thấp (BMI = 16.4 kg/m2). Không có chứng tăng sắc tố điển hình của bệnh Addison. Tuyến giáp không to lên và chức năng giáp bình thường. Khám tim mạch và hô hấp bình thường. Có loạn dưỡng mỡ dưới da nhẹ ở vị trí tiêm insulin.
Kết quả sinh hóa có liên quan khác: albumin 4.0 g/dl (3.8 – 4.8 g/dl), AST 10U/L (14 – 50 U/L), ALA 10U/L (10-55 U/L) , gama – glutamin transferase 30 U/L (10 – 70 U/L) và creatinine 0.6 mg/dl hay 53 micromol/L (0.7 – 1.4 mg/dL hay 65 -125 micromol/L). Nồng độ insulin và peptide C đo tại 1 trong các cơn hạ glucose (glucose tĩnh mạch 2.8 mmol/L) trong lần nhập viện này là 83.6 mU/L (0.0 – 25.0 mU/L) và 36 pmol/L (364 – 1655 pmol/L) và sinh hóa tuyến giáp của bệnh nhân bình thường.
THẢO LUẬN:
Hạ đường huyết là một biến chứng thường gặp của liệu pháp insulin ở bệnh nhân ĐTĐ và gây cản trở mục tiêu kiểm soát đường huyết. Nó gây ra bệnh lý về thể chất và tinh thần nghiêm trọng, thỉnh thoảng gây tử vong. Nguyên nhân cơ bản của hạ đường huyết cần được đánh giá và xác định nhằm ngăn chặn các cơn hạ đường huyết tái phát.
Hạ glucose máu ở bệnh nhân ĐTĐ thông thường nhất là được gây ra bởi liệu pháp insulin quá mức tuyệt đối hay tương đối. Những nguyên nhân của quá mức insulin tuyệt đối bao gồm quá mức hoặc chất kích thích tiết insulin không đúng lúc; hoặc quá mức insulin; hoặc do giảm thải insulin trong suy thận. Insulin quá mức tương đối xảy ra khi lượng insulin hiện tại không tương xứng với lượng glucose cung cấp (ngoại sinh), sử dụng hoặc sản xuất. Dư thừa quá mức insulin tuyệt đối hay tương đối luôn dễ dàng nhận ra từ bệnh sử bệnh nhân thông qua các biểu hiện trước đó các đợt hạ đường huyết. Sau khi kiểm tra tiền sử bệnh chi tiết của BN này, dư thừa insulin không là nguyên nhân của các cơn hạ glucose. Vì liều insulin ở bệnh nhân là phù hợp với lượng calo thu nhận hằng ngày và bệnh nhân đủ khả năng để tiêm chính xác liều insulin. Bệnh nhân đã không tự ý sử dụng thêm insulin. Loạn dưỡng mỡ tại nơi tiêm có thể ảnh hưởng hấp thu insulin và là nguyên nhân thông thường gây bất thường nồng độ glucose. Bệnh nhân này chỉ bị loạn lưỡng mỡ nhẹ, và thay đổi vị trí tiêm đã không cải thiện được các cơn hạ glucose máu tái phát. Do đó, loại trừ nguyên nhân này.
Suy gan và suy thận được loại trừ qua khám lâm sàng và các xét nghiệm nồng độ men gan, albumin và creatinin trong giới hạn bình thường. Suy giảm tuyến thượng thận, đặc biệt là bệnh
Addison ở bệnh nhân đái thái đường type I có thể gây hạ glucose máu. Kiểm tra ACTH cho thấy nồng độ đỉnh của cortisol là 34.8 microgram/dL (960 mmol/L) [đáp ứng bình thường : >20 microgram/dL (> 550 mmol/L)] và đã loại trừ chẩn đoán đó. Bệnh nhân không dùng alcohol, và không đang dùng các thuốc gây ra hạ glucose máu (trừ insulin).
Chứng liệt dạ dày ở bệnh nhân ĐTĐ (chiếm tỷ lệ 30-40% ở bệnh nhân ĐTĐ) là tình trạng đặc trưng bởi sự chậm làm rỗng dạ dày không có tắc ruột cơ học do bệnh lý thần kinh tự động. Tình trạng này có thể gây hạ glucose máu do sự chậm tiêu thức ăn khiến lượng insulin cung cấp và carbohydrate hấp thu là không tương xứng. Một khảo sát về tình trạng làm rỗng dạ dày đã được thực hiện trên bệnh nhân cho thấy bệnh nhân có tình trạng này. Tuy nhiên, biểu hiện chứng tăng glucose sau ăn 2-3h (đặc biệt sau ăn tối), theo đó là sự giảm glucose máu giữa đêm là không phù hợp với chứng liệt dạ dày, nên nguyên nhân này được loại trừ.
Sau khi loại trừ các nguyên nhân thông thường của chứng hạ glucose máu ở bệnh nhân ĐTĐ sử dụng liệu pháp insulin, tiến hành các khảo sát khác sâu hơn trên bệnh nhân này để tìm ra nguyên nhân của hạ đường huyết tái phát. Nồng độ insulin và peptide C đã được đo trong các đợt hạ glucose xảy ra. Nồng độ peptide C không phát hiện được trong 3 cơn hạ glucose riêng biệt đã loại trừ khả năng bệnh nhân bị tăng insulin nội sinh, ví dụ u đảo tụy.
Sau khi loại trừ các nguyên nhân trên, kháng thể kháng insulin (IA) được cân nhắc là nguyên nhân trong bối cảnh nồng insulin tăng khi cơn hạ glucose xảy ra. Sử dụng lâu dài insulin ngoại sinh có thể làm tăng kháng thể kháng insulin, các kháng thể này gắn kết với Insulin. Bởi vậy, liều insulin đồng dạng (insulin analog) lớn hơn có thể được yêu cầu để bù cho lượng insulin gắn kết và cho phép lượng insulin tự do có đủ để hoạt động. Insulin tự do và insulin gắn kết tồn tại cân bằng động với nhau. Khi dạng tự do được chuyển hóa, insulin ở dạng gắn kết sẽ được giải phóng từ IA. Điều này có tác dụng làm chậm và kéo dài hoạt động insulin ban đầu và gây tăng glucose máu ban ngày; ngươc lại, sự giải phóng insulin tiếp theo từ IA có thể gây hạ glucose máu về đêm nếu lượng insulin giải phóng không cân xứng với lượng calo nhận vào.
IA đặc trưng bởi dung lượng gắn kết và ái lực gắn kết. Những bệnh nhân có IA có dung lượng gắn kết thấp, ái lực cao thường không bị gây hạ glucose máu. Trái lại, các bệnh nhân với IA có dung lượng gắn trung bình, ái lực thấp có thể gặp cơn hạ glucose máu về đêm. Còn các bệnh nhân với IA có dung lượng gắn cao, ái lực thấp có nguy cơ gặp cơn tăng glucose nghiêm trọng ban ngày và hạ glucose ban đêm, và có thể cần chữa trị với thuốc ức chế miễn dịch.
IA có thể xem như là một chất cản trở insulin (do tạo đại phân tử insulin dạng phức hợp IA- Insulin). Tuy nhiên, không như các chất cản trở các hormone khác, đánh giá phi tuyến tính bằng cách pha loãng các mẫu xét nghiệm của bệnh nhân hay kiểm tra lại nồng độ insulin trên các mẫu xét nghiệm thay thế là không hữu ích để nghiên cứu IA ở các bệnh nhân ĐTĐ sử dụng liệu pháp insulin. Bởi vì hầu hết mẫu insulin xét nghiệm không thể hiện sự hồi quy tuyến tính với insulin analog và có phản ứng chéo khác nhau đối với loại insulin analog khác nhau. Vì lý do này, đánh giá hồi quy sau khi thêm insulin vào mẫu xét nghiệm là không phù hợp.
Sắc ký đồ dạng gel có thể được dùng để chứng thực chẩn đoán của insulin dạng phức hợp IA- Insulin và do đó khẳng định sự hiện diện của IA, thể hiện bằng đỉnh insulin trên vùng globulin miễn dịch. IA cũng có thể được đo trực tiếp. Những xét nghiệm này thông thường không có sẳn tại đa số phòng labo. Khi nghi ngờ có IA, đo lường nồng độ insulin tự do,insulin trực tiếp và insulin tổng. Insulin trực tiếp (direct insulin) được đo trực tiếp trên mẫu máu gốc từ bệnh nhân. Insulin tự do (free insulin) thu được bằng cách đo phần nổi trên bề mặt sau khi lắng đọng mẫu máu bằng polyethylen glycol (PEG). Insulin tổng (total insulin) thu bằng cách: đầu tiên, thêm acid vào mẫu máu để tách phần insulin gắn kết kháng thể thành dạng tự do, các bước tiếp theo lần lượt là lắng đọng mẫu máu bằng thêm PEG và trung hòa pH.
Ở người bình thường, insulin tổng , insulin tự do, insulin trực tiếp có nồng độ gần bằng nhau, vì insulin trong hệ tuần hoàn gắn protein không đáng kể. Do đó, sự tăng tỉ lệ insulin trực tiếp/tự do, hoặc tỷ lệ insulin tổng cộng/trực tiếp là gợi ý có sự tồn tại của IA. Những tỉ lệ này có tính đặc hiệu phụ thuộc tùy vào máy phân tích. Ở bệnh nhân này, tỉ lệ insulin trực tiếp/tự do và tỷ lệ insuin tổng/trực tiếp tương ứng là 1.03 và 0.98, sử dụng máy xét nghiệm Advia Centaur (Siemens Healthcare Diagnostic). Đo trực tiếp nồng độ IA được 0.01 nmol/L (giá trị bình thường: không lớn hơn 0.02 nmol/L, Mayo Medical Laboratories). Những kết quả này loại trừ IA là nguyên nhân gậy hạ glucose máu.
Vì nguyên nhân của hạ glucose máu tái phát vẫn chưa tìm ra, chúng tôi đo insulin và glucose trong 24h của bệnh nhân. Insulin trong 24h cho thấy đỉnh bất thường giữa lúc 24h – 2h30, điều này phù hợp với sự hạ glucose nghiêm trọng lúc đó (1.9 mmol/L). Đỉnh này không thể giải thích bằng phác đồ kê insulin cho bệnh nhân (Hình 1). Chúng tôi nghi ngờ rằng đỉnh này có thể do một chất tương tự insulin (insulin analog) tác động ngắn đã được tiết ra một cách âm thầm. Sau khi giải thích kết quả insulin 24h cho bệnh nhân, cơn hạ glucose máu về đêm đã không xảy ra nữa. BN sau đó được chuyển sang khoa tâm thành để được chăm sóc và phát hiện BN có những yếu tố gây stress khá nghiêm trọng.
Chúng tôi đi đến quyết định rằng bệnh nhân này mắc chứng hạ glucose máu giả tạo (factitious hypoglycemia) – một hội chứng mà bệnh nhân tự cảm ứng gây hạ glucose để nhằm được chăm
sóc y tế hoặc để chứng tỏ là mình không khỏe. Đây là một chứng bệnh rất khó chẩn đoán và thường không chẩn đoán được trong nhiều năm ở bệnh nhân bị ĐTĐ không kiểm soát được. Các biểu hiện lâm sàng thường bắt chước rất giống với bệnh thật. Bệnh nhân thường tỏ ra lo lắng và yêu cầu thường xuyên được kiểm tra cũng như can thiệp điều trị. BN thường có tiền sử nhiều lần nhập viện và đến khám nhiều nơi khác nhau. Bệnh nhân này cũng đã vào viện nhiều lần, cụ thể:18 lần trong vòng 2 năm do hạ glucose tái phát và tăng glucose máu.
Điều quan trọng là phải nhận ra đây là một chẩn đoán loại trừ và chỉ nên thực hiện sau khi loại trừ các nguyên nhân có khả năng khác trước đó để tránh nhầm lẫn trong chẩn đoán – để tránh các hậu quả nghiêm trọng về xã hội, pháp lý và lâm sàng do chẩn đoám sai. Tuy nhiên, việc cẩn thận này cũng cần phải cân bằng với sự cần thiết phải nhận biết sớm để tránh các chẩn đoán và can thiệp điều trị không cần thiết – gây lãng phí vật chất cũng như đem nguy hại cho bệnh nhân. (Hình 2).
Hình 2. Các phương pháp nào giúp chẩn đoán các nguyên nhân gây hạ glucose máu tái phát ở bệnh nhân đái tháo đường
NHỮNG ĐIỀU CẦN NHỚ:
1. Chứng hạ glucose máu là thông thường ở bệnh nhân ĐTĐ và nguyên nhân thường gặp nhất là sự dư thừa insulin tuyệt đối hay tương đối. Loạn dưỡng mỡ dưới da tại nơi tiêm có thể tác động tới sự hấp thu insulin và có thể làm nồng độ glucose không ổn định. Chậm tháo rỗng dạ dày (30%-40% ở bệnh nhân ĐTĐ) gây ra bởi liệt dạ dày có thể gây hạ glucose máu.
2. Kháng thể kháng insulin và việc lén lút sử dụng insulin ngoại sinh có thể làm tăng nồng
độ insulin bất hợp lí trong hạ glucose máu.
3. Hạ glucose máu giả tạo là thách thức lớn với chẩn đoán và điều trị. Nó nên được xem là một chẩn đoán phân biệt trong hạ glucose máu không rõ nguyên nhân và là một chẩn đóan loại trừ (chẩn đoán khẳng định sau khi đã loài trừ các nguyên nhân khác).
4. Đo lường nồng độ peptide C và insulin trực tiếp và tự do có thể giúp phân biệt hạ glucose giả tạo với các nguyên nhân khác.
5. Nồng độ insulin cao với sự tăng tỉ lệ insulin trực tiếp/tự do ghi lại trong các cơn hạ glucose gợi ý một nguyên nhân là do lạm dụng insulin. (Lời bình của người hiệu đính: theo như cách hiểu logic thì nồng độ insulin cao và tỷ lệ insulin trực tiếp/tự do xấp xỉ 1 trong các cơn hạ glucose gợi ý một nguyên nhân là do lạm dụng insulin. Còn nồng độ insulin cao và tỷ lệ insulin trực tiếp/tự do tăng thì nghi ngờ nguy cơ là do IA ?).

Các yếu tố nguy cơ gây ung thư vú(P2)
Các nguy cơ gây ung thư vú(P2)
2. Lối sống và nguy cơ ung thư vú
Có con
Nguy cơ mắc ung thư vú tăng nhẹ ở những phụ nữ không có con hoặc có con đầu lòng sau tuổi 30. Mang thai nhiều lần và mang thai khi còn trẻ làm giảm nguy cơ ung thư vú. Tuy vậy, ảnh hưởng của việc mang thai đối với các loại ung thư vú khác nhau thì khác nhau. Với một số thể ung thư vú , việc mang thai làm tăng nguy cơ ung thư.
Biện pháp ngừa thai
Biện pháp ngừa thai
Thuốc tránh thai đường uống: Các nghiên cứu cho thấy nguy cơ mắc ung thư vú tăng nhẹ ở những phụ nữ sử dụng thuốc tránh thai đường uống so với người chưa từng sử dụng các thuốc này. Nguy cơ này dường như trở lại bình thường khi dừng thuốc. Với người dừng sử dụng thuốc hơn 10 năm, nguy cơ ung thư vú không thay đổi so với bình thường. Khi cân nhắc sử dụng thuốc tránh thai đường uống, nên thảo luận về các yếu tố nguy cơ gây ung thư vú với cán bộ y tế.
Depot-medro xyprogesteron acetat (DMPA; Depo-Provera) là một progesteron dạng tiêm được sử dụng 3 tháng 1 lần để phòng tránh thai. Một vài nghiên cứu cho thấy ảnh hưởng của DMPA trên nguy cơ ung thư vú. Phụ nữ trong thời gian sử dụng DMPA có nguy cơ mắc ung thư vú cao hơn, tuy nhiên nguy cơ mắc ung thư dường như không tăng lên khi dừng sử dụng thuốc trên 5 năm.
Liệu pháp bổ sung hormon thời kì phụ nữ mãn kinh
Liệu pháp sử dụng estrogen (thường kết hợp với progesteron) được sử dùng từ nhiều năm này để giảm triệu chứng mãn kinh và ngăn ngừa loãng xương. Các nghiên cứu trước đây đề xuất rằng nó có thể có các lợi ích khác cho sức khỏe, tuy nhiên các lợi ích này không được tìm thấy gần đây qua các nghiên cứu được thiết kế tốt hơn. Liệu pháp này được gọi bằng nhiều tên như liệu pháp hormon sau mãn kinh (post-menopausal hormone therapy), liệu pháp hormon thay thế (hormone replacement therapy) và liệu pháp hormon mãn kinh (menopausal hormon therapy).
Có 2 loại liệu pháp hormon chính. Với người còn tử cung, bác sĩ thường kê đơn cả estrogen và progesteron (được gọi là liệu pháp hormon kết hợp). Progesteron rất cần thiết do estrogen đơn độc làm tăng nguy cơ ung thư tử cung. Với người không còn tử cung (người đã từng phẫu thuật cắt tử cung), có thể kê estrogen đơn độc. Liệu pháp này thường được gọi là liệu pháp thay thế estrogen hoặc liệu pháp estrogen.
Các nghiên cứu cho thấy sử dụng liệu pháp hormon kết hợp sau khi mãn kinh làm tăng nguy cơ mắc ung thư vú. Nó cũng tăng nguy cơ tử vong do ung thư vú.
Sử dụng estrogen đơn độc sau mãn kinh không làm tăng nguy cơ mắc ung thư vú.
Cho con bú
Một số nghiên cứu cho kết quả gợi ý rằng việc cho con bú làm giảm nhẹ nguy cơ mắc ung thư vú, đặc biệt nếu cho bú liên tục từ 1,5 đến 2 năm. Tuy nhiên, điều này rất khó để nghiên cứu, đặc biệt ở các quốc gia như Mỹ, nơi mà việc cho bú trong thời gian dài không phải là phổ biến.
Ảnh hưởng này có thể do việc cho con bú làm giảm số lượng chu kỳ kinh nguyệt trong cuộc đời của người phụ nữ (tương tự với việc bắt đầu chu kỳ kinh nguyệt muộn hoặc sớm).
Rượu
Sử dụng rượu có mối liên hệ rõ ràng với việc tăng nguy cơ mắc ung thư vú. Nguy cơ tăng lên tỷ lệ với lượng rượu tiêu thụ. So sánh với người không uống rượu, người uống 1 cốc rượu tiêu chuẩn một ngày có nguy cơ tặng rất ít. Người uống từ 2 đến 5 cốc mỗi ngày có nguy cơ cao hơn 1,5 lần so với người không uống rượu. Uống nhiều rượu cũng làm tăng nguy cơ mắc một số loại ung thư khác.
Quá cân hoặc béo phì
Quá cân hoặc béo phì sau mãn kinh làm tăng nguy cơ ung thư vú. Trước mãn kinh, buồng trứng sinh ra phần lớn estrogen trong cơ thể, và mô mỡ sinh ra một lượng nhỏ. Sau mãn kinh (khi buồn trừng dừng sản xuất estrogen), phần lớn estrogen có nguồn gốc từ mô mỡ. Tăng mô mỡ sau khi mãn kinh có thể làm tăng nguy cơ mắc ung thư vú do tăng nồng độ estrogen. Tương tự, những phụ nữ quá cân thường có nồng độ insulin trong máu cao hơn. Nồng độ insulin cao cũng có thể liên quan tới một số ung thư, bao gồm cả ung thư vú.
Tuy nhiên, quan hệ giữa cân nặng và nguy cơ ung thư vú rất phức tạp. Ví dụ, nguy cơ ung thư tăng lên ở những phụ nữ tăng cân ở tuổi trưởng thành nhưng có thể không tăng ở những người quá cân khi còn nhỏ. Tương tự, quá nhiều mỡ ở vùng eo có thể ảnh hưởng tới nguy cơ ung thư vú nhiều hơn cùng lượng mỡ đó ở vùng hông và đùi. Các nhà nghiên cứu tin rằng các tế bào mô mỡ ở các vùng khác nhau của cơ thể có sự khác biệt, điều này có thể giải thích cho sự ảnh hưởng phức tạp trên.
Hoạt động thể lực
Ngày càng có nhiều bằng chứng cho thấy hoạt động thể lực dưới dạng các bài tập thể dục làm giảm nguy cơ ung thư vú. Câu hỏi chính là cường độ cần thiết là bao nhiêu. Trong một nghiên cứu từ Cơ quan sáng kiến về sức khỏe phụ nữ, đi bộ nhanh khoảng 1,25 đến 2,5 giờ trên tuần làm giảm nguy cơ ung thư khoảng 18%/người. Đi bộ 10 giờ/tuần giảm nguy cơ hơn một chút nữa.
3. Các yếu tố chưa rõ
Chế độ ăn và vitamin
Nhiều nghiên cứu đã tìm hiểu mối liên hệ giữa chế độ ăn và nguy cơ ung thư vú, nhưng đến nay các kết quả vẫn còn nhiều mâu thuẫn. Một số nghiên cứu cho thấy chế độ ăn có thể đóng một vai trò trong sự phát triển ung thư, trong khi các nghiên cứu khác lại không thấy bằng chứng rằng chế độ ăn ảnh hưởng tới nguy cơ ung thư vú. Ví dụ, một nghiên cứu thấy rằng phụ nữ ăn nhiều thịt đỏ hơn có nguy cơ ung thư vú cao hơn.
Các nghiên cứu cũng chú ý tới nồng độ vitamin, và cũng thu được kết quả không thống nhất. Một số nghiên cứu hiện nay thấy rằng ở phụ nữ có nồng độ cao một số chất dinh dưỡng, nguy cơ ung thư vú tăng lên. Đến nay, không có nghiên cứu nào cho thấy rằng sử dụng vitamin làm giảm nguy cơ ung thư vú. Điều này không có nghĩa chế độ ăn lành mạnh không có lợi ích gì. Một chế độ ăn ít béo, ít các loại thịt đỏ và thịt qua chế biến, nhiều rau và hoa quả có thể có các lợi ích khác với sức khỏe.
Phần lớn nghiên cứu cho thấy rằng ung thư vú ít phổ biến hơn ở các nước nơi chế độ ăn điển hình là ít các loại chất béo, ít chất béo không bão hòa đa (polyunsaturated fat) và ít chất béo bão hòa. Tuy nhiên nhiều nghiên cứu về phụ nữ tại Mỹ không thấy mối liên quan giữa ung thư vú và lượng chất béo đưa vào cơ thể. Các nhà nghiên cứu vẫn không chắc chắn về lời giải thích cho sự mâu thuẫn này. Ít nhất chế độ ăn cũng ảnh hưởng một phần tới cân nặng của cơ thể. Tương tự, các nghiên cứu so sánh chế độ ăn và nguy cơ ung thư ở các nước khác cũng cho kết quả phức tạp do bị ảnh hưởng bởi các yếu tố như mức độ vận động, lượng các chất dinh dưỡng khác và gen.
Cần có thêm nghiên cứu để đánh giá ảnh hưởng của các loại chất béo với nguy cơ ung thư vú. Nhưng chắc chắn rằng lượng calo có liên quan và chất béo là nguồn calo chính. Chế độ ăn nhiều chất béo dẫn tới quá cân hoặc béo phì (là yếu tố nguy cơ gây ung thư vú), đồng thời ảnh hưởng tới sự phát triển của một số loại ung thư khác. Lượng chất béo sử dụng (một số loại) ảnh hưởng rõ ràng tới nguy cơ bệnh tim.
Các hóa chất trong môi trường
Nhiều nghiên cứu đã và đang được thực hiện để đánh giá ảnh hưởng của môi trường lên nguy cơ ung thư vú.
Các hợp chất trong môi trường có tính chất tương tự estrogen được đặc biệt quan tâm, ví dụ, các hợp chất trong một số loại nhựa, một số mỹ phẩm và sản phẩm chăm sóc cá nhân, thuốc trừ sâu (như DDE), và các polychlorinat biphenyl (PCB). Các chất này theo lý thuyết có thể ảnh hưởng tới nguy cơ ung thư vú.
Vấn đề này là mối quan tâm lớn của cộng đồng, nhưng ở thời điểm này các nghiên cứu không cho thấy mối liên hệ rõ ràng giữa nguy cơ ung thư vú và sự phơi nhiễm với các chất này. Đáng tiếc rằng khó thực hiện các nghiên cứu về loại ảnh hưởng này ở người. Cần có thêm nghiên cứu để xác định ảnh hưởng tới sức khỏe của các chất này và các chất tương tự.
Hút thuốc lá
Trong một thời gian dài, các nghiên cứu không tìm thấy mối liên hệ giữa hút thuốc và ung thư vú. Trong những năm gần đây, nhiều nghiên cứu đã thấy rằng nghiện thuốc lá nặng trong thời gian dài có liên quan với sự gia tăng nguy cơ ung thư vú. Một số nghiên cứu cho thấy nguy cơ lớn nhất là ở những phụ nữ bắt đầu hút thuốc trước khi có con đầu lòng. Báo cáo của Hội bác sĩ phẫu thuật Mỹ năm 2014 về việc hút thuốc kết luận rằng bằng chứng “có tính gợi ý nhưng không đầy đủ” rằng hút thuốc làm tăng nguy cơ ung thư vú.
Một trọng tâm nghiên cứu hiện nay là việc hút thuốc thụ động có tăng nguy cơ ung thư vú hay không. Cả khói thuốc khi hút thuốc trực tiếp hay gián tiếp đều chứa các chất hóa học gây ung thư vú ở loài gặm nhấm ở nồng độ cao. Các chất hóa học trong khói thuốc tới mô tuyến vú và bài tiết ra sữa.
Bằng chứng nghiên cứu về mối quan hệ nữa hút thuốc thụ động và nguy cơ ung thư vú ở người còn gây tranh cãi, ít nhất một phần nào đó do mối quan hệ này còn chưa rõ ràng. Có thể giải thích cho điều này là khói thuốc lá có thể ảnh hưởng khác nhau với nguy cơ ung thư vú trên người hút thuốc và người chỉ phơi nhiễm với khói thuốc.
Một báo cáo từ Phòng bảo vệ môi trường California năm 2005 kết luận rằng bằng chứng cho thấy chắc chắn có mối quan hệ nhân quả giữa hút thuốc thụ động và nguy cơ ung thư vú ở người trẻ, đặc biệt phụ nữ trước mãn kinh. Báo cáo của Hiệp hội bác sĩ phẫu thuật năm 2004 lại kết luận rằng không có bằng chứng chắc chắn về mối liên hệ này. Trong bất kỳ trường hợp nào, nguy cơ này đủ để có lý do tránh việc hút thuốc thụ động.
Làm việc đêm
Một số nghiên cứu cho thấy rằng phụ nữ làm việc về đêm (như y tá ca đêm) có thể có nguy cơ mắc ung thư vú cao hơn. Gần đây, nhiều nghiên cứu hơn được tiến hành về vấn đề này. Một số nhà nghiên cứu nghĩ rằng ảnh hưởng này có thể do sự thay đổi nồng độ melatonin, một hormon được bài tiết thay đổi dựa theo sự phơi nhiễm của cơ thể với ánh sáng, tuy nhiên các hormon khác cũng đang được nghiên cứu.
4. Các yếu tố còn tranh cãi hoặc chưa được chứng minh
Chất chống đổ mồ hồi
Tin đồn trên internet và e-mail cho rằng các chất hóa học chống đổ mồ hôi dưới cánh tay được hấp thụ qua da, vào hệ bạch huyết, gây độc cho quá trình phát triển của tuyến vú và cuối cùng dẫn tới ung thư vú.
Dựa trên các bằng chứng hiện nay (bao gồm kiến thức về cơ chế hoạt động của cơ thể), có rất ít lý do để tin rằng các chất chống đổ mồ hồi làm tăng nguy cơ ung thư vú.
Áo ngực
Tin đồn qua internet và e-mail và ít nhất một quyển sách cho rằng áo ngực gây ung thư vú do gây tắc nghẽn dòng bạch huyết. Không có cơ sở khoa học hay lâm sàng cho khẳng định này, và một nghiên cứu gần đây gồm 1500 phụ nữ cho thấy không có mối liên hệ giữa việc sử dụng áo ngực với nguy cơ ung thư vú.
Phá thai
Một số nghiên cứu cho dữ liệu chắc chắn rằng cả phá thai và xảy thai đều không có ảnh hưởng tới nguy cơ ung thư vú.
Cấy ghép vú
Một số nghiên cứu cho thấy rằng việc cấy ghép vú không làm tăng nguy cơ ung thư vú, mặc dù đặt túi silicon có thể gây mô sẹo trong vú. Việc cấy ghép có thể gây khó khăn để quan sát mô vú trong phim chụp x-quang chuẩn của vú, nhưng khi sử dụng hình ảnh thêm (additional x-ray pictures) , được gọi là hình ảnh thay thế cấy ghép (implant displacement view) có thể thăm khám mô vú một cách đầy đủ.
Cấy ghép vú có thể gây lymphoma thể hiếm gọi là lymphoma thểtế bào lớn thoái biến. Biến thể lymphoma này hiếm khi được thấy ở mô vú quanh nơi cấy ghép. Tới nay, có rất ít ca đã biết cho thấy nguy cơ mắc thể lymphoma này cao hơn ở những phụ nữ cấy ghép ngực.
Xem các nguy cơ ung thư vú phần 1 tại đây

Các yếu tố nguy cơ gây ung thư vú(P1)
Các yếu tố nguy cơ gây ung thư vú
Yếu tố nguy cơ là yếu tố ảnh hưởng tới khả năng bị bệnh. Các loại ung thư khác nhau có các yếu tố nguy cơ khác nhau. Ví dụ, da tiếp xúc với ánh sáng mặt trời cường độ mạnh là một yếu tố nguy cơ gây ung thư da. Hút thuốc là yếu tố nguy cơ gây ung thư phổi, miệng, thanh quản, bàng quang, thận và một số cơ quan khác.
Tuy nhiên yếu tố nguy cơ không cho biết tất cả. Có một hoặc thậm chí một vài yếu tố nguy cơ không có nghĩa rằng bạn sẽ mắc bệnh. Phần lớn những phụ nữ có một hoặc một vài yếu tố nguy cơ gây ung thư vú không bao giờ mắc bệnh, trong khi nhiều phụ nữ mắc ung thư trong khi không có yếu tố nguy cơ nào (ngoài việc là một phụ nữ và đang già đi). Thậm chí khi một người phụ nữ có các nguy cơ mắc ung thư, cũng khó để biết rằng cần phải có bao nhiêu yếu tố để mắc bệnh.
Một số yếu tố nguy cơ, như tuổi và chủng tộc, không thể thay đổi. Các nguy cơ khác liên quan tới các yếu tố gây ung thư từ môi trường, từ thói quen như hút thuốc, uống rượu, chế độ ăn. Một số yếu tố gây nguy cơ cao hơn các yếu tố khác và nguy cơ bị mắc ung thư vú có thể thay đổi theo thời gian do các yếu tố như tuổi và lối sống.
1. Yếu tố nguy cơ không thể thay đổi
Giới tính
Giới tính ảnh hưởng nguy cơ ung thư vú
Giới tính nữ là yếu tố nguy cơ chính gây ung thư vú. Nam giới có thể mắc ung thư vú nhưng căn bệnh này phổ biến ở nữ hơn 100 lần so với nam. Điều này có thể do nam giới có ít hormon nữ (estrogen và progesteron) hơn trong khi các hormon này có thể thúc đẩy sự phát triển của tế bào ung thư vú.
Tuổi
Nguy cơ phát triển ung thư vú tăng lên theo độ tuổi. Khoảng 1/8 ca ung thư xâm lấn xảy ra ở phụ nữ dưới 45 tuổi trong khi 2/3 số ca ở phụ nữ trên 55 tuổi.
Yếu tố di truyền
Khoảng 5-10% ca ung thư vú được cho là di truyền, có nghĩa là ung thư là kết quả trực tiếp từ các sai sót trong bộ gen (đột biến) di truyền từ bố hoặc mẹ.
ADN là một chất hóa học tồn tại trong mỗi tế bào của cơ thể, tạo nên bộ gen – mã hóa cho các chức năng của tế bào. Chúng ta thường trông giống với cha mẹ do cha mẹ là nguồn gen của chúng ta. Tuy vậy ADN không chỉ ảnh hưởng tới vẻ ngoài.
Một số gen quy định khi nào các tế bào sinh trưởng, nhân đôi thành các tế bào mới và chết đi. Gen làm tăng nhanh sự nhân đôi các tế bào được gọi là oncogen. Các gen làm chậm quá trình nhân đôi hoặc gây chết các tế bào vào thời gian thích hợp, được gọi là các gen ức chế khối u. Một số biến đổi (đột biến) trong ADN gây hoạt hóa các oncogen hoặc bất hoạt các gen ức chế khối u có thể biến tế bào tuyến vú bình thường trở thành tế bào ung thư.
Đột biến di truyền
Một số đột biến ADN di truyền có thể tăng đột ngột nguy cơ phát triển ung thư và là nguyên nhân gây ra ung thư di truyền trong gia đình. Ví dụ, gen BRCA (BRCA1 và BRCA2) là các gen ức chế khối u. Đột biến ở một trong số các gen này có thể được di truyền từ bố mẹ. Khi một trong số các gen này bị đột biến, không còn yếu tố ức chế sự phát triển bất thường, ung thư có nguy cơ phát triển hơn.
Hiện nay, phụ nữ đã bắt đầu được hưởng lợi ích từ việc hiểu được cơ sở di truyền của ung thư vú. Xét nghiệm gen có thể xác định người có đột biến di truyền trên gen ức chế khối u BRCA1 hoặc BRCA2 (hoặc hiếm hơn là đột biến trên gen khác như PTEN hoặc TP53). Những người này có thể áp dụng các biện pháp để giảm thiểu nguy cơ phát triển của ung thư vú và theo dõi sự thay đổi ở tuyến vú một cách thận trọng để phát hiện ung thư ở giai đoạn sớm, có khả năng chữa trị cao hơn.
Đột biến trên các gen ức chế khối u như BRCA được xem là có độ thâm nhập cao do những thay đổi này thường dẫn tới ung thư. Mặc dù nhiều phụ nữ mang đột biến có độ thâm nhập cao mắc ung thư, hầu hết các ca ung thư (kể cả ung thư vú) không gây ra bởi loại đột biến này. Thông thường, các đột biến hoặc biến đổi gen có độ thâm nhập thấp là các yếu tố trong sự phát triển của ung thư. Mỗi một đột biến trên có tác động nhỏ trên sự phát triển ung thư của mỗi cá nhân nhưng tác động tổng thể trên quần thể có thể lớn do các đột biến này phổ biến và mọi người thường chịu ảnh hưởng bởi nhiều đột biến cùng một lúc hơn là chỉ một đột biến. Các gen này có thể ảnh hưởng tới nồng độ hormon, chuyển hóa hoặc các yếu tố liên quan tới nguy cơ ung thư vú. Các gen này có thể là nguyên nhân gây ung thư mang tính di truyền.
Đột biến gen mắc phải
Phần lớn đột biến ADN liên quan tới ung thư vú thường xảy ra đơn độc trên tế bào tuyến vú trong cuộc đời người phụ nữ hơn là do di truyền. Các đột biến “mắc phải” trên oncogen và/hoặc gen ức chế khối u có thể là kết quả từ các yếu tố khác như bức xạ hoặc các chất hóa học gây ung thư. Tuy nhiên cho tới hiện tại, nguyên nhân gây ra phần lớn các đột biến mắc phải này còn chưa được xác định. Phần lớn bệnh nhân ung thư vú có một vài đột biến gen mắc phải.
Xét nghiệm đột biến điểm mắc phải có thể giúp bác sĩ đánh giá chính xác hơn tình trạng ung thư vú. Ví dụ, xét nghiệm có thể xác định những người mắc ung thư vú có quá nhiều oncogen HER2, với những trường hợp này ung thư có xu hướng ác tính hơn. Đồng thời các thuốc được phát triển với đích tác dụng đặc biệt trên loại ung thư này và đã được chứng minh hiệu quả.
BRCA1 và BRCA2:
Nguyên nhân thường gặp nhất gây ung thư vú mang tính di truyền là đột biến di truyền trên gen BRCA1 và BRCA2. Ở các tế bào thường, các gen này giúp ngăn ngừa ung thư bằng cách tổng hợp các protein ngăn tế bào phát triển bất thường. Người mang bản sao đột biến của các gen này di truyền từ bố mẹ có nguy cơ cao mắc ung thư cao hơn trong suốt cuộc đời.
Mặc dù ở một số gia đình mang gen đột biến BRCA1, nguy cơ ung thư vú trong suốt cuộc đời khoảng 80%, trong khi trung bình nguy cơ này nằm trong khoảng 55 – 65%. Với gen BRCA2 đột biến, nguy cơ mắc bệnh thấp hơn, khoảng 45%.
Ung thư vú có liên quan tới các đột biến này thường xảy ra hơn ở phụ nữ trẻ và thường ảnh hưởng tới cả 2 bên vú hơn các loại ung thư không liên quan tới các đột biến này. Những phụ nữ mang các đột biến này cũng có nguy cơ cao hơn phát triển các ung thư khác, đặc biệt là ung thư buồng trứng.
Ở Mỹ, đột biến trên gen BRCA phổ biến ở người Do Thái có nguồn gốc Ashkenazi (Đông Âu) hơn các nhóm chủng tộc và dân tộc khác, tuy vậy điều này có thể xảy ra ở bất kỳ ai.
Biến đổi các gen khác: Các đột biến gen khác cũng có thể dẫn tới ung thư vú di truyền. Các đột biến gen này hiếm hơn nhiều và thường không làm tăng nguy cơ ung thư vú nhiều như đột biến trên gen BRCA và không phải nguyên nhân thường gặp của ung thư vú di truyền.
ATM: Gen ATM thường giúp sửa chữa các ADN bị hư hại. Thừa hưởng 2 bản sao bất thường của gen này gây chứng mất điều hòa giãn mạch. Thừa hưởng một bản sao gen đột biến gây tăng tỷ lệ ung thư vú ở một số gia đình.
TP53: Gen TP53 là khuôn mẫu để tổng hợp protein p53 giúp ngăn cản sự tăng trưởng bất thường của tế bào. Đột biến di truyền của gen này gây hội chứng Li-Fraumeni (được đặt tên theo 2 nhà nghiên cứu đầu tiên mô tả hội chứng này). Bệnh nhân mắc hội chứng này có nguy cơ mắc ung thư vú cao hơn, cũng như một số bệnh ung thư khác như ung thư bạch cầu, u não và sarcoma (ung thư xương hoặc mô liên kết). Đây là nguyên nhân gây ung thư vú hiếm gặp.
CHEK2: Hội chứng Li-Fraumeni cũng có thể do đột biến di truyền ở gen CHEK2. Thậm chí khi đột biến không gây hội chứng này, nó vẫn có thể tăng nguy cơ ung thư vú khoảng 2 lần.
PTEN: Gen PTEN giúp điều hòa sự tăng trưởng của tế bào. Đột biến di truyền ở gen này gây hội chứng Crowden, một rối loạn hiếm gặp. Những người mắc hội chứng này có nguy cơ mang khối u lành tính và ác tính cao hơn, như khối u trong đường tiêu hóa, tuyến giáp, tử cung và buồng trứng. Khiếm khuyết ở gen này cũng gây một hội chứng khác được gọi là Bannayan-Riley-Ruvalcaba được cho là không ảnh hưởng tới nguy cơ ung thư vú. Gần đây các hội chứng gây ra do PTEN được gộp thành một hội chứng gọi là hội chứng PTEN Tumor Hamartoma.
CDH1: Các đột biến di truyền ở gen này gây ung thư dạ dày lan tỏa di truyền, đây là một hội chứng trong đó ung thư dạ dày thể hiếm phát triển ở người trẻ tuổi. Phụ nữ mang các đột biến trên gen này cũng có nguy cơ cao hơn mắc ung thư tiểu thùy tuyến vú xâm lấn.
STK11: Khiếm khuyết ở gen này có thể dẫn tới hội chứng Peutz-Jeghers. Bệnh nhân mắc hội chứng này xuất hiện các đốm màu trên môi và trong miệng, polyp ở ống nước tiểu và ống tiêu hóa, và có nguy cơ cao mắc nhiều loại ung thư, bao gồm cả ung thư vú.
PALB2: Gen PALB2 tổng hợp protein liên kết với protein được tổng hợp dựa trên gen BRCA2. Khiếm khuyết (đột biến) trên gen này có thể dẫn tới tăng nguy cơ mắc ung thư vú. Chưa rõ rằng các đột biến trên gen PALB2 có làm tăng nguy cơ ung thư buồng trứng và ung thư vú ở nam giới hay không.
Xét nghiệm gen:
Xét nghiệm gen có thể được thực hiện để tìm kiếm đột biến trên gen BRCA1 và BRCA2 (hoặc một số gen khác liên quan tới nguy cơ mắc ung thư vú). Mặc dù xét nghiệm có thể có ích trong một số trường hợp, tuy nhiên cần xem xét thận trọng lợi ích và tác hại.
Tiền sử gia đình về ung thư vú
Ở những người phụ nữ mà trong gia đình có người quan hệ huyết thống gần mắc bệnh, nguy cơ mắc bệnh sẽ cao hơn.
Nguy cơ mắc ung thư vú tăng khoảng 2 lần khi có quan hệ huyết thống trong phạm vi 1 thế hệ với người mắc bệnh (mẹ, chị hoặc con gái), tăng lên khoảng 3 lần khi có quan hệ huyết thống trong phạm vi 2 thế hệ với người mắc bệnh.
Ở những phụ nữ có cha hoặc anh trai bị ung thư vú, không xác định được chính xác nguy cơ mắc ung thư vú nhưng nguy cơ mắc bệnh ở những người này cũng cao hơn. Nói chung, dưới 15% phụ nữ mắc ung thư vú có thành viên trong gia đình mắc bệnh. Điều này có nghĩa là phần lớn (hơn 85%) phụ nữ mắc ung thư vú không có tiền sử gia đình mắc bệnh.
Tiền sử ung thư vú của bản thân
Những phụ nữ mắc ung thư một bên vú có nguy cơ mắc ung thư mới ở bên vú còn lại hoặc phần khác của bên vú đó cao hơn 3-4 lần. Điều này khác với tái phát ung thư ban đầu.
Chủng tộc và dân tộc
Nhìn chung, phụ nữ da trắng thường mắc ung thư vú nhiều hơn phụ nữ Mỹ gốc phi, nhưng phụ nữ Mỹ gốc phi thường tử vong do ung thư vú nhiều hơn. Tuy nhiên, ở phụ nữ dưới 45 tuổi, ung thư vú phổ biến ở người Mỹ gốc phi hơn. Người châu Á, Tây Ban Nha, Bồ Đào Nha, thổ dân châu Mỹ có nguy cơ mắc ung thư vú và tử vong thấp hơn.
Mô tuyến vú đặc
Tuyến vú được tạo thành từ mô mỡ, mô xơ và mô tuyến. Một số người có mô tuyến vú đặc (quan sát trên phim chụp x-quang), tức là có nhiều mô tuyến và mô xơ, ít mô mỡ hơn. Người có tuyến vú đặc trên phim chụp x-quang có nguy cơ ung thư vú cao hơn 1,2 đến 2 lần so với người có mật độ vú trung bình. Tuy nhiên, mô vú đặc cũng khiến phim chụp kém chính xác hơn.
Một số yếu tố có thể ảnh hưởng tới mật độ vú, như tuổi, giai đoạn mãn kinh, một số thuốc (bao gồm liệu pháp hormon thay thế ở giai đoạn mãn kinh), mang thai và gen.
Một số tình trạng u vú lành tính
Người mang u tuyến vú lành tình có thể có nguy cơ ung thư vú cao hơn. Một số ảnh hưởng tới nguy cơ ung thư vú hơn những tình trạng còn lại. Bác sĩ thường chia u vú lành tình thành 3 nhóm chính, phụ thuộc vào sự ảnh hưởng của nó tới nguy cơ ung thư vú.
Thương tổn không tăng sinh: Các loại u vú lành tính này không đi kèm với sự tăng sinh mô tuyến vú. Các tình trạng này không ảnh hưởng tới nguy cơ ung thư vú, nếu có thì ảnh hưởng trong phạm vi rất nhỏ. Nhóm này bao gồm:
Xơ hóa và/hoặc nang đơn thuần (thường được gọi là bệnh xơ nang)
Tăng sản nhẹ
Bệnh tuyến không xơ cứng (adenosis)
Phình ống dẫn sữa
Bướu diệp thể (lành tính)
U nhú đơn độc
Hoại tử mô mỡ
Xơ hóa quanh ống dẫn sữa
Dị sản thể có vẩy và thể tiết rụng đầu.
Vôi hóa quanh biểu mô
Các khối u lành tính khác (lipoma, hamartoma, hemangioma, neurofibroma, adenomyoethelioma)
Mastitis (viêm vú) không phải một thương tổn, tuy nhiên đây là tình trạng có thể xảy ra mà không làm tăng nguy cơ mắc ung thư vú.
Thương tổn có tăng sản (không thuộc thể không điển hình): Các tình trạng này có sự tăng sinh quá mức ở ống dẫn sữa hoặc tiểu thùy ở mô tuyến vú, làm tăng nhẹ nguy cơ mắc ung thư vú ở phụ nữ (1,5-2 lần). Nhóm này bao gồm:
Tăng sản ống dẫn sữa thường (không phải typ không điển hình)
U sợi tuyến vú
Bệnh tuyến xơ cứng
Một vài u nhú (gọi là papillomatosis)
Sẹo hình ngôi sao
Thương tổn tăng sản không điển hình: Trong các trường hợp này, có sự tăng sinh của tế bào ở ống dẫn sữa hoặc tiểu thùy của mô tuyến vú, trong đó một số tế bào không còn ở trạng thái bình thường. Các tổn thương này ảnh hưởng lớn tới nguy cơ ung thư vú, làm tăng nguy cơ lên 3,5-5 lần. Các loại tổn thương này bao gồm:
Tăng sản ống dẫn sữa không điển hình
Tăng sản tiểu thùy không điển hình
Phụ nữ có tiền sử gia đình ung thư vú, đồng thời bị mắc chứng tăng sản hoặc tăng sản không điển hình có nguy cơ mắc ung thư vú cao hơn nhiều.
Ung thư biểu mô tiểu thùy tại chỗ (LCIS – Lobular carcinoma in situ)
Trong LCIS, các tế bào giống tế bào ung thư phát triển trong tiểu thùy tuyến tiết sữa, tuy nhiên chúng không phát triển xuyên qua thành tiểu thùy. LCIS (còn được gọi là lobular neoplasia) thường được xếp vào nhóm ung thư vú không xâm lấn cùng với ung thư biểu mô ống dẫn sữa (DCIS – ductal carcinoma in situ) tại chỗ, tuy nhiên khác với DCIS ở chỗ nó không trở thành ung thư xâm lấn khi không điều trị.
Phụ nữ mắc tình trạng này có nguy cơ mắc ung thư xâm lấn gấp 7-11 lần ở cả 2 vú. Do đó, người mắc LCIS nên thường xuyên kiểm tra x-quang vú và thăm khám bác sĩ.
Chu kỳ kinh nguyệt
Nguy cơ mắc ung thư vú tăng nhẹ ở những phụ nữ có chu kỳ kinh nguyệt bắt đầu sớm (trước 12 tuổi) và/hoặc mãn kinh muộn (sau 55 tuổi). Mức độ tăng nguy cơ mắc bệnh có thể phụ thuộc vào thời gian phơi nhiễm với hormon estrogen và progesteron.
Tiền sử xạ trị
Nguy cơ mắc ung thư vú tăng đáng kể ở phụ nữ có tiền sử xạ trị ở vùng ngực để điều trị các loại ung thư khác (như lymphoma) khi còn nhỏ hoặc còn trẻ. Nguy cơ này thay đổi theo tuổi của bệnh nhân vào thời điểm xạ trị. Nếu đồng thời sử dụng hóa trị, buồng trứng có thể dừng sản xuất hormon trong một thời gian, điều này làm giảm nguy cơ mắc ung thư vú. Nguy cơ mắc ung thư vú do xạ trị cao nhất khi việc điều trị được thực hiện vào tuổi thiếu niên, khi tuyến vú đang phát triển. Xạ trị sau tuổi 40 dường như không làm tăng nguy cơ ung thư vú.
Tiền sử phơi nhiễm diethylstilbestrol
Từ những năm 1940 đến 1960, một số phụ nữ sử dụng thuốc diethylstilbestrol (DES) trong thời kỳ mang thai do thuốc này được cho là giảm nguy cơ xảy thai. Nguy cơ mắc ung thư vú ở những người này tăng nhẹ so với bình thường. Con của những người này cũng có nguy cơ mắc ung thư vú cao hơn.
Xem tiếp các nguy cơ ung thư vú phần 2: tại đây
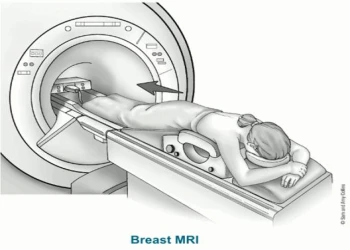
Cộng hưởng từ tuyến vú
Cộng hưởng từ tuyến vú
Hội ung thư Mĩ khuyến cáo những phụ nữ có nguy cơ cao mắc ung thư vú nên tầm soát bằng cộng hưởng từ tuyến vú (MRI) cùng với chụp nhũ ảnh định kỳ hàng năm. MRI không được khuyến khích dùng như một công cụ tầm soát riêng biệt, vì mặc dù nhạy nhưng nó vẫn có thể phát hiện sót một số ung thư mà nhũ ảnh có thể phát hiện. MRI cũng được dùng trong một vài trường hợp khác, như để kiểm tra kỹ hơn những vùng khả nghi được tìm thấy qua nhũ ảnh hoặc nhìn kỹ hơn tuyến vú ở người được chẩn đoán mắc ung thư vú.
Cộng hưởng từ tuyến vú
Quét MRI dùng sóng điện từ và sóng vô tuyến thay cho tia X quang để đưa ra những hình ảnh chi tiết các lớp cắt ngang của cơ thể. Những kiểm tra MRI hữu ích nhất là dùng một chất cản quang (gadolinium) tiêm vào ống thông đặt trong tĩnh mạch (IV) cánh tay trước hoặc trong khi kiểm tra. Điều này giúp nâng cao chất lượng MRI nhằm cho thấy một cách rõ ràng các cấu trúc mô vú.
Mặc dù MRI có thể tìm thấy các ung thư không phát hiện được bằng nhũ ảnh, nhưng cũng nhiều khả năng những thứ tìm được không phải là ung thư (dương tính giả). Kết quả dương tính giả phải được kiểm tra để biết chắc rằng không có ung thư, nghĩa là phải làm thêm kiểm tra và/hoặc sinh thiết. Đây là lý do MRI không được khuyến khích dùng để sàng lọc ung thư vú ở những phụ nữ có nguy cơ trung bình mắc ung thư vú, vì phương pháp này có thể dẫn đến những sinh thiết không cần thiết và nhiều kiểm tra khác ở phần lớn những người này.
MRI tuyến vú khá tốn kém, cần được xác nhận bởi công ty bảo hiểm trước khi thực hiện. Đa số những bảo hiểm tư nhân chi trả cho tầm soát nhũ ảnh cũng có khả năng sẽ chi trả cho MRI nếu người bệnh cho thấy được mình đang có nguy cơ cao mắc bệnh. Điều này cho phép họ có thể đến một phòng khám cho người có nguy cơ cao, nơi có nhân viên nhiều kinh nghiệm, để được chấp thuận cho chụp MRI tuyến vú.
Yêu cầu khi thực hiện MRI vú
Quét MRI có thể tốn nhiều thời gian – thường là 1 giờ. Để MRI tuyến vú, bệnh nhân phải nằm trong một ống hẹp, nằm úp sấp trên bàn máy được thiết kế đặc biệt. Bàn máy hở ở mỗi bên vú để có thể chụp mà không bị chèn ép. Bàn máy có bộ cảm biến để chụp lại các hình ảnh. Nằm yên, giữ nguyên tư thế trong suốt quá trình chụp là rất quan trọng.
Nằm bên trong ống này có thể khiến người ta bức bối và khó chịu do chứng sợ không gian hẹp (sợ không gian khép kín). Thiết bị cũng tạo ra tiếng ù lớn và tiếng lách cách có thể quấy rầy bệnh nhân. Một số nơi sẽ cho bệnh nhân nghe nhạc bằng tai nghe để loại bỏ những âm thanh này.
Nguồn: Hội ung thư Mỹ

Cách khám ngực lâm sàng
Hiện nay căn bệnh ung thư vú đang khá phổ biến với phụ nữ. Và để xác định sớm được bệnh nhân có bị bệnh vú hay không các bác sĩ thường xuyên sử dụng phương pháp khám ngực lâm sàng để có thể chẩn đoán sơ bộ được tình trạng bệnh của bệnh nhân.
Khám ngực lâm sàng
Khám ngực lâm sàng
Khám ngực lâm sàng (CBE) là một trong những loại hình kiểm tra sức khỏe được thực hiện bởi những chuyên gia chăm sóc sức khỏe như: bác sĩ, chuyên viên điều dưỡng thực hành, điều dưỡng, kỹ thuật viên. Cụ thể, bạn phải cởi trần từ phần eo trở lên. Tiếp theo, các chuyên gia sức khỏe sẽ xem xét sự bất thường về kích thước và hình dáng của cặp ngực hay sự thay đổi của da ở vùng ngực và núm vú. Sau đó, dùng mặt thịt trong của các ngón tay để sờ nắn nhẹ nhàng trực tiếp trên ngực.
Cần đặc biệt chú ý đến hình dạng và kết cấu của ngực, vị trí các khối u, dù khối u trên da hoặc các khối u nằm sâu trong các mô. Khu vực dưới hai cánh tay cũng cần được kiểm tra.
Khám ngực lâm sàng là cơ hội giúp cho các chị em phụ nữ học hỏi phương pháp kiểm tra ngực từ các chuyên gia sức khỏe. Hãy yêu cầu bác sĩ và điều dưỡng hướng dẫn bạn cách tự khám ngực một cách chính xác và theo dõi để điều chỉnh thao tác của bạn.
Nguồn: Hội ung thư Mỹ

Khuyến cáo Hiệp hội ung thư Hoa Kì về phát hiện sớm ung thư vú
Khuyến cáo của Hiệp hội Ung thư Hoa Kỳ để phát hiện sớm ung thư vú ở bệnh nhân không có triệu chứng
Khuyến cáo của hội ung thư hoa kì
Phụ nữ từ 40 tuổi trở lên nên thực hiện chụp X-quang tuyến vú (chụp nhũ ảnh) hàng năm và duy trì việc này ngay cả khi sức khoẻ vẫn còn tốt.
Các bằng chứng gần đây ủng hộ lợi ích của chụp nhũ ảnh đã tăng lên đáng kể. Đặc biệt, chụp nhũ ảnh rất có ý nghĩa với phụ nữ ở độ tuổi 40 trong việc phát hiện ung thư sớm. Tuy nhiên, việc chụp nhũ ảnh cũng có một vài hạn chế nhất định, đó là không phát hiện được một số loại ung thư hoặc đưa ra chẩn đoán nhầm.
Bệnh nhân cần được phổ biến về những lợi ích và hạn chế của việc thực hiện chụp nhũ ảnh từ sớm. Mặc dù có những hạn chế nhất định, chụp nhũ ảnh vẫn là một phương pháp hiệu quả và có giá trị trong việc giảm nguy cơ mắc và tử vong vì ung thư vú.
Chụp nhũ ảnh cần được duy trì và không phụ thuộc vào độ tuổi của bệnh nhân, miễn là bệnh nhân không có bệnh lý nghiêm trọng hay kéo dài nào như suy tim sung huyết, bệnh thận giai đoạn cuối, bệnh phổi tắc nghẽn mãn tính và mất trí nhớ trung bình đến nghiêm trọng. Tuổi không phải là lý do để ngừng thực hiện chụp nhũ ảnh định kì. Những bệnh nhân có vấn đề nghiêm trọng về sức khoẻ hoặc tuổi thọ ngắn cần thảo luận với bác sĩ về việc có nên tiếp tục thực hiện chụp nhũ ảnh hay không.
Phụ nữ ở độ tuổi 20-30 cần thực hiện khám lâm sàng tuyến vú định kì 3 năm/lần bởi một bác sĩ chuyên khoa. Khi bước sang tuổi 40, họ cần được thăm khám hàng năm.
Khám lâm sàng được thực hiện cùng với chụp nhũ ảnh là cơ hội để bệnh nhân và bác sĩ hay y tá của họ thảo luận về những thay đổi ở tuyến vú, phát hiện sớm và xác định các yếu tố ở tiền sử của bệnh nhân có thể khiến cho họ dễ mắc ung thư vú.
Việc khám lâm sàng tuyến vú trước khi chụp nhũ ảnh có một vài lợi ích nhất định. Việc thăm khám thường bao gồm những hướng dẫn để bệnh nhân làm quen với tuyến vú của chính họ. Theo đó, họ được phổ biến về những lợi ích và hạn chế của việc thăm khám lâm sàng tuyến vú cũng như việc tự khám ngực. Khả năng mắc ung thư vú rất thấp ở bệnh nhân trong độ tuổi 20 và nguy cơ này tăng dần theo độ tuổi. Do đó, bệnh nhân cần thông báo bất cứ triệu chứng nào bất thường ở tuyến vú của họ cho bác sĩ.
Tự thăm khám tuyến vú (tự khám ngực) nên được bắt đầu ở những phụ nữ ở độ tuổi 20. Họ cần được giải thích về những lợi ích và hạn chế của việc tự khám ngực và phải báo cáo ngay lập tức bất kì thay đổi nào ở tuyến vú cho bác sĩ.
Các nghiên cứu đã chỉ ra rằng tự thăm khám tuyến vú có ít vài trò phát hiện ung thư vú hơn so với việc tình cờ phát hiện ra khối u vú hoặc đơn giản là người phụ nữ tự cảm nhận được các dấu hiệu thông thường. Một số cảm thấy thoải mái với việc tự thăm khám thường xuyên (hàng tháng sau chu kì) theo phương pháp từng bước có hệ thống để quan sát và cảm nhận ngực của họ. Một số khác lại thích cảm nhận ngực của họ khi tắm hoặc mặc đồ hay thực hiện kiểm tra không thường xuyên.
Đôi lúc bệnh nhân quá chú tâm vào việc “làm thế này đã đúng chưa” và bị lo lắng khi thực hiện tự khám ngực. Tuy nhiên, tự khám ngực chỉ là cách mà bệnh nhân biết được ngực của họ trông như thế nào cũng như cảm nhận và phát hiện các thay đổi. Mục đích cuối cùng vẫn là thông báo ngay lập tức những thay đổi bất thường ở tuyến vú cho bác sĩ hoặc y tá của họ dù có thực hiện tự khám ngực hay không.
Những phụ nữ quyết định tự thực hiện thăm khám tuyến vú cần được một chuyên gia y tế hướng dẫn kĩ thuật thăm khám. Họ có thể chọn thực hiện việc này một lần mỗi tháng hoặc không. Tuy nhiên, khi thăm khám thường xuyên, họ sẽ biết được tuyến vú tuông thường sẽ trông như thế nào và nhanh chóng nhận ra bất cứ sự thay đổi nào. Nếu có một thay đổi xuất hiện, ví dụ như tăng kích thước bầu ngực, sưng, kích ứng vùng da ngực, đau núm vú, tụt núm vú (núm vú di chuyển vào bên trong bầu ngực), đỏ hay tiết dịch bất thường (không phải sữa mẹ - quan sát thấy trên áo ngực), bệnh nhân cần đến khám bác sĩ càng sớm càng tốt. Tuy nhiên, những thay đổi này chưa phải là triệu chứng của ung thư.
Phụ nữ có nguy cơ mắc ung thư vú cao dựa trên một số yếu tố nguy cơ nhất định nên được chụp cộng hưởng từ và chụp X-quang tuyến vú hàng năm.
Các đối tượng này bao gồm:
Có nguy cơ của ung thư vú từ 20% đến 25% hoặc cao hơn theo các công cụ đánh giá nguy cơ dựa vào tiền sử gia đình (như mô hình Claus - xem dưới đây)
Mang gen đột biến BRCA1 hoặc BRCA2
Người thân (bố, mẹ, anh, chị, em hoặc con) có gen đột biến BRCA1 hoặc BRCA2 và chưa thực hiện kiểm tra gen
Phải xạ trị vùng ngực trong độ tuổi từ 10-30
Mắc hội chứng Li-Fraumeni, Cowden hoặc Bannayan-Riley-Ruvalcaba, hoặc người thân (mẹ hay chị em) mắc những hội chứng này
Hiệp hội ung thư Hoa Kỳ không khuyến cáo sử dụng sàng lọc bằng chụp cộng hưởng ở những phụ nữ mà nguy cơ ung thư vú nhỏ hơn 15%.
Hiện nay chưa có đủ bằng chứng để khuyến cáo sử dụng hay không biện pháp sàng lọc bằng chụp cộng hưởng ở những phụ nữ có nguy cơ ung thư vú trung bình (nguy cơ ước tính từ 15-20% theo thang đánh giá dựa trên tiền sử của gia đình) hoặc những người có thể có nguy cơ ung thư vú cao dựa trên một số yếu tố nguy cơ như:
Có tiền sử mắc ung thư vú, ung thư biểu mô tuyến vú tại chỗ (DCIS), ung thư tiểu thùy tại chỗ (LCIS), tăng sản tuyến vú không điển hình (ADH), hoặc tăng sản lobular không điển hình (ALH)
Mật độ mô ngực cao hoặc dày đặc trên nhũ ảnh
Nếu sử dụng chụp cộng hưởng, nên cân nhắc kết hợp sàng lọc bằng nhũ ảnh, bởi vì mặc dù chụp cộng hưởng nhạy hơn (nghĩa là khả năng phát hiện khối u cao hơn nhũ ảnh) nhưng cũng có một số trường hợp chụp cộng hưởng không phát hiện được những khối u có thể nhìn thấy trên nhũ ảnh.
Đối với hầu hết phụ nữ có nguy cơ cao, sàng lọc bằng chụp cộng hưởng và nhũ ảnh nên được bắt đầu ở độ tuổi 30 và duy trì miễn là bệnh nhân có sức khoẻ tốt. Tuy nhiên do chưa có đủ bằng chứng về độ tuổi thích hợp nhất để bắt đầu sàng lọc, quyết định đưa ra sẽ căn cứ vào sự thảo luận giữa bệnh nhân và bác sĩ dựa trên tình trạng và mong muốn của họ.
Rất nhiều công cụ đánh giá nguy cơ, ví dụ như mô hình của Gail, Claus hay Tyrer-Cuzich được các chuyên gia y tế sử dụng để đánh giá nguy cơ mắc ung thư vú ở bệnh nhân. Những cộng cụ này cho phép ước tính một cách tương đối, chứ không chính xác nguy cơ mắc ung thư vú dựa trên rất nhiều các yếu tố nguy cơ và số liệu khác nhau.
Bởi vì các công cụ khác nhau sử dụng các yếu tố khác nhau để ước tính nguy cơ nên chúng có thể đưa ra những ước tính khác nhau trên cùng một đối tượng bệnh nhân. Ví dụ, mô hình của Gail đánh giá dựa trên các yếu tố nguy cơ của bệnh thể như tuổi, tuổi có kinh nguyệt (thời kỳ có kinh nguyệt lần đầu tiên), tiền sử sinh thiết vú trước đó cùng tiền sử ung thư vú của người thân ở thế hệ đầu tiên. Ngược lại, mô hình của Claus ước tính nguy cơ mà chỉ dựa trên tiền sử mắc ung thư vú ở người thân cả hai thế hệ đầu tiên và thứ hai. Hai mô hình này rất dễ đưa ra những ước tính khác nhau trên cùng một bệnh nhân.
Các công cụ đánh giá nguy cơ (ví dụ như mô hình của Gail) do không dựa hoàn toàn trên tiền sử của gia đình nên không phù hợp để sử dụng cùng với các khuyến cáo của Hiệp hội ung thư Hoa Kỳ để xác định bệnh nhân có nên thực hiện sàng lọc bằng chụp cộng hưởng từ hay không. Việc sử dụng bất kì một công cụ đánh giá nguy cơ nào và kết quả thu được cần được thảo luận bởi bệnh nhân và bác sĩ.
Bệnh nhân nữ được sàng lọc bằng chụp cộng hưởng từ được khuyến cáo làm sinh thiết cùng lúc nếu có thể. Nếu không thực hiện, họ sẽ cần chụp cộng hưởng từ thêm một lần nữa khi làm sinh thiết.
Chưa có bằng chứng nào cho thấy chụp cộng hưởng từ là một phương pháp sàng lọc có hiệu quả ở bệnh nhân nữ có nguy cơ trung bình. Mặc dù chụp cộng hưởng từ nhạy hơn nhũ ảnh, phương pháp này lại có tỷ lệ chẩn đoán dương tính sai cao hơn (dễ phát hiện nhầm những vật thể không phải khối u). Việc này có thể dẫn đến phải thực hiện những xét nghiệm sinh thiết và những xét nghiệm khác không cần thiết ở những phụ nữ đã được sàng lọc và gây ra những lo lắng và sợ hãi không đáng có.
Hiệp hội ung thư Mỹ tin rằng việc thực hiện chụp X-quang, cộng hưởng từ (ở phụ nữ có nguy cơ cao), khám lâm sàng tuyến vú, phát hiện và báo cáo những thay đổi ở tuyến vú từ sớm theo những khuyến cáo nêu trên sẽ giúp bệnh nhân giảm thiểu nguy cơ tử vong vì ung thư vú. Việc tuân thủ các khuyến cáo này có ý nghĩa hơn bất kì một thăm khám hay xét nghiệm đơn độc nào.
Không thể phủ nhận việc khám lâm sàng tuyến vú mà không tiến hành chụp nhũ ảnh có thể để sót những khối u vú quá nhỏ mà bệnh nhân hoặc bác sĩ không cảm nhận được nhưng lại có thể nhìn thấy trên nhũ ảnh. Chụp nhũ ảnh là một phương pháp rà soát khá nhạy, tuy nhiên một số khối u không hiện trên nhũ ảnh nhưng lại có thể được cảm nhận bởi bệnh nhân hoặc bác sĩ. Với những phụ nữ có nguy cơ mắc ung thư vú cao, ví dụ như những người có đột biến gen BRCA hoặc tiền sử gia đình có người mắc, việc chụp cộng hưởng kết hợp chụp X- quang tuyến vú được khuyến cáo thực hiện.
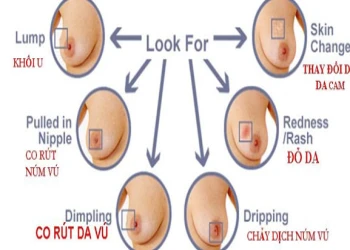
Các dấu hiệu của bệnh ung thư vú
Các dấu hiệu ung thư vú và triệu chứng của bệnh.
Việc áp dụng rộng rãi phương pháp chụp X-quang tuyến vú đã giúp phát hiện ngày càng nhiều ca ung thư vú ngay cả trước khi chúng gây ra các triệu chứng điển hình. Tuy nhiên, vẫn có một số trường hợp ung thư vú không phát hiện được bằng phương pháp này do không thực hiện việc kiểm tra, hoặc thậm chí được thực hiện trong điều kiện lý tưởng, phương pháp này vẫn không phát hiện ra được khối u.
X-quang tuyến vú
Triệu chứng phổ biến nhất của ung thư vú là xuất hiện khối u. Một khối u không đau, cứng, bờ không đều, có nguy cơ cao là dấu hiệu của ung thư. Trong khi đó, khối u của ung thư vú có thể mềm hơn, tròn hơn và có thể gây đau. Do vậy, việc kiểm tra kịp thời các khối u và các thay đổi ở vú với các bác sĩ chuyên khoa là hết sức cần thiết.
Các dấu hiệu khác của ung thư vú, bao gồm:
Sưng tấy một phần hay cả ngực. (ngay cả khi chưa khối u nào được phát hiện rõ ràng)
Kích ứng da hay xuất hiện các vết lõm.
Đau vú và núm vú.
Đầu vú bị thụt vào trong
Ửng đỏ, xuất hiện vảy hoặc da dày lên ở vú hoặc núm vú
Tiết dịch núm vú.
Dấu hiệu ung thư vú
Trong một số trường hợp, khối u của ung thư vú có thể lan tới các hạch bạch huyết dưới nách và xung quanh xương cổ, rồi tạo thành bướu ở các vị trí đó, thậm chí trước khi các khối u gốc ở các mô vú đủ lớn để cảm nhận.
Các triệu chứng trên có thể xuất hiện do các bệnh khác. Khi bạn có một trong các triệu chứng trên, tốt nhất nên gặp bác sĩ kịp thời để tìm hiểu rõ nguyên nhân.
Nguồn: Hội ung thư Mỹ
Ung thư vú là gì?
Ung thư vú là gì?
Ung thư vú là khối u ác tính bắt nguồn từ các tế bào vú. Một khối u ác tính là tập hợp các tế bào ung thư có thể phát triển xâm lấn các mô xung quanh hoặc di căn tới các mô xa hơn trong cơ thể. Ung thư vú hầu hết xảy ra ở phụ nữ, tuy nhiên nam giới cũng có thể mắc bệnh.
Tài liệu này chỉ đề cập tới ung thư vú ở phụ nữ.
Cấu trúc bình thường của tuyến vú
Để hiểu về ung thư vú, cần biết một số kiến thức cơ bản về cấu trúc bình thường của tuyến vú (trong hình dưới đây).
Tuyến vú của phụ nữ được hình thành từ các tiểu thùy (tuyến tiết sữa), ống dẫn (các ống nhỏ dẫn sữa từ tiểu thùy tới núm vú) và mô đệm (mô mỡ và mô liên kết xung quanh các ống dẫn và tiểu thùy, các mạch máu và mạch bạch huyết)
Ung thư vú phần lớn bắt nguồn từ các tế bào ống dẫn (ung thư ống dẫn). Một số bắt nguồn từ tế bào tiểu thùy (ung thư tiểu thùy), chỉ một lượng nhỏ bắt nguồn từ các mô khác.
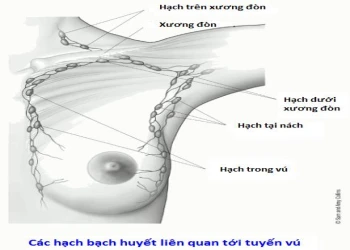
Hệ bạch huyết của tuyến vú
Hiểu biết về hệ thống bạch huyết rất quan trọng vì đây có thể là một con đường lan tỏa của ung thư vú. Hệ thống này gồm một số bộ phận.
Hạch bạch huyết nhỏ, hình hạt đậu, là tập hợp của các tế bào miễn dịch (các tế bào đóng vai trò quan trọng trong quá trình chống lại sự nhiễm trùng), các hạch bạch huyết này được kết nối với nhau bằng các mạch bạch huyết. Mạch bạch huyết là các tĩnh mạch nhỏ, không chứa máu mà chứa một chất lỏng trong suốt ra khỏi tuyến vú, được gọi là bạch huyết. Bạch huyết chứa dịch mô và các chất thải cũng như các tế bào của hệ thống miễn dịch. Các tế bào ung thư vú có thể đi vào mạch bạch huyết và phát triển trong các hạch bạch huyết.
Phần lớn các mạch bạch huyết trong vú đều liên kết với các hạch bạch huyết dưới cánh tay ( nodes- hạch bạch huyết ở nách). Một số mạch bách huyết nối với hạch bạch huyết bên trong ngực (internal mammary nodes – Hạch bạch huyết trong vú) và các hạch ở trên hoặc dưới xương đòn (supraclavicular nodes – hạch bạch huyết trên xương đòn hoặc infraclavicular nodes – hạch bạch huyết dưới xương đòn).
Nếu các tế bào ung thư lan tỏa tới các hạch bạch huyết, có nguy cơ cao các tế bào này cũng có thể đi vào máu và di căn tới các vị trí khác của cơ thể. Tế bào ung thư lan tỏa tới càng nhiều hạch bạch huyết, ung thư càng tồn tại ở nhiều cơ quan khác của cơ thể. Do đó, việc tìm thấy ung thư ở một hay nhiều hạch bạch huyết thường ảnh hưởng tới kế hoạch điều trị. Tuy nhiên, không phải ở tất cả các bệnh nhân có tế bào ung thư vú tại hạch bạch huyết đều dẫn tới di căn và có những trường hợp không có tế bào ung thư tại hạch bạch huyết nhưng vẫn xuất hiện di căn sau đó.
U lành tính tại tuyến vú
Phần lớn các bướu tại vú không phải ung thư. Tuy nhiên, một số trường hợp cần được sinh thiết (lấy mẫu và quan sát dưới kính hiển vi) để chắc chắn không phải ung thư.
Xơ nang tuyến vú
Phần lớn các bướu được gây ra bởi sự xơ hóa và/hoặc các nang, đây là các biến đổi lành tính trong mô tuyến vú xảy ra ở một thời điểm nào đó trong cuộc đời ở nhiều phụ nữ (thường được gọi là xơ hóa hay bệnh xơ hóa). Xơ hóa là quá trình hình thành mô xơ (giống sẹo) trong khi các nang là các túi chứa dịch. Các tình trạng này thường được bác sĩ chẩn đoán dựa trên các triệu chứng như bướu tại vú, sưng, căng, đau. Các triệu chứng này tăng lên ngay trước chu kỳ kinh nguyệt. Có thể cảm thấy vú có các u cục và đôi khi có thể thấy dịch trong hoặc hơi đục chảy ra từ núm vú.
U sợi tuyến vú và u nhú nội ống dẫn sữa
Các khối u lành tính tại vú như "u sợi tuyến vú" hoặc "u nhú nội ống dẫn sữa" là sự phát triển bất thường nhưng không phải ung thư và không di căn tới các cơ quan khác bên ngoài tuyến vú. Các khối u này không đe dọa tính mạng.
Tuy nhiên, cần quan tâm đến tình trạng u lành tính tại vú do những phụ nữ này có nguy cơ hình thành ung thư vú cao hơn những người khác.
Nguồn: Hội Ung thư Mỹ
DS Nguyễn Thị Minh Trang
Tìm hiểu về Ung Thư
Ung thư là tên gọi chung cho một nhóm gồm hơn 100 bệnh khác nhau. Mặc dù có nhiều loại ung thư khác nhau nhưng tất cả đều có đặc điểm chung là bắt nguồn từ việc tế bào tăng sinh bất thường không kiểm soát được. Ung thư không được điều trị có thể dẫn đến tử vong.
Tế bào ung thư
Các tế bào bình thường trong cơ thể
Cơ thể được tạo thành từ hàng triệu tế bào sống. Các tế bào bình thường lớn lên, phân chia và chết theo chu trình. Trong suốt những năm đầu đời, tế bào bình thường phân chia nhanh hơn cho phép cơ thể lớn lên. Sau khi trưởng thành, phần lớn các tế bào chỉ phân chia để thay thế các tế bào lão hóa hoặc tế bào chết hoặc để làm lành vết thương.
Ung thư bắt đầu như thế nào?
Ung thư bắt đầu khi các tế bào ở một bộ phận nào đó của cơ thể tăng sinh không kiểm soát được. Sự phát triển của các tế bào ung thư khác so với tế bào bình thường. Thay vì chết đi, các tế bào ung thư tiếp tục phát triển và tạo thành các tế bào bất thường mới. Các tế bào ung thư cũng phát triển và xâm lấn sang các mô khác. Tăng sinh không kiểm soát và xâm lấn sang mô khác là đặc điểm nổi bật của tế bào ung thư.
Các tế bào trở thành tế bào ung thư vì ADN bị tổn thương. ADN là phân tử chứa các gen được mã hóa, có mặt ở mọi tế bào và điều khiển mọi hoạt động của tế bào. Ở tế bào bình thường, khi ADN bị tổn thương thì tế bào hoặc sửa chữa ADN hoặc chết đi. Ở tế bào ung thư, ADN bị tổn thương không được sửa chữa và tế bào cũng không chết đi. Thay vào đó, tế bào tiếp tục phát triển và tạo thành những tế bào mới mà cơ thể không cần. Tất cả những tế bào mới này đều có ADN bị tổn thương như tế bào bất thường ban đầu.
Một người có thể có ADN bất thường (di truyền từ bố mẹ), nhưng phần lớn ADN bị tổn thương là lỗi xảy ra khi tế bào bình thường đang sao chép hoặc bởi tác động từ môi trường. Đôi khi, nguyên nhân của việc tổn thương ADN có thể là hút thuốc lá hoặc phơi nhiễm với ánh sáng mặt trời. Nhưng hiếm khi chúng ta biết được chính xác nguyên nhân gây ung thư.
Phần lớn các trường hợp, tế bào ung thư tạo thành một khối u (bướu). Qua thời gian, các khối u này có thể thay thế tế bào bình thường, chèn ép hoặc đẩy các tế bào bình thường về một phía. Một vài loại ung thư, như ung thư bạch cầu, hiếm khi tạo thành các khối u. Thay vào đó, các tế bào ung thư này ảnh hưởng đến máu và cơ quan tạo máu và lan sang các mô khác khi chúng phát triển.
Ung thư phát triển như thế nào?
Các tế bào ung thư thường đi qua các bộ phận khác của cơ thể - nơi mà chúng có thể phát triển và tạo thành mô mới (quá trình này gọi là ung thư di căn). Điều này xảy ra khi các tế bào ung thư xâm nhập vào máu hoặc hạch bạch huyết. Ung thư có thể phát triển ở bất cứ đâu, nó được gọi theo tên của nơi tế bào ung thư được phát hiện đầu tiên. Ví dụ, ung thư ruột di căn đến gan gọi là ung thư ruột đã di căn, không phải ung thư gan. Trong trường hợp này, các tế bào ung thư ở gan cũng giống như các tế bào ung thư ở ruột. Chúng sẽ được điều trị như nhau.
Các loại ung thư khác nhau thế nào?
Các loại ung thư khác nhau được điều trị khác nhau. Ví dụ, ung thư phổi và ung thư da là hai bệnh khác nhau. Chúng phát triển ở tỷ lệ khác nhau và đáp ứng với các phương pháp điều trị khác nhau. Điều này giải thích tại sao bệnh nhân ung thư cần điều trị đúng với loại ung thư mà bệnh nhân mắc phải.
Khối u không phải ung thư
Một khối u là một bướu hoặc tập hợp các tế bào bất thường, nhưng không phải tất cả các khối u đều là ung thư. Các khối u không phải ung thư được gọi là u lành. U lành có thể gây ra các vấn đề: chúng phát triển rất rộng và chèn ép lên các mô và cơ quan khỏe mạnh. Nhưng chúng không xâm lấn sang các mô khác. Vì chúng không thể xâm lấn nên chúng cũng không thể lây lan sang các cơ quan khác của cơ thể (không di căn). Những khối u này hầu như không đe dọa đến tính mạng.