Mvasi 400mg/16ml (Bevacizumab) - Thuốc điều trị ung thư hiệu quả của Mỹ
21,100,000 đ
Chính sách khuyến mãi
Dược sỹ tư vấn 24/7.
Khách hàng lấy sỉ, sll vui lòng liên hệ call/Zalo để được cập nhật giá
Sản phẩm chính hãng, cam kết chất lượng.
Kiểm tra hàng trước khi thanh toán.
Chuyển phát toàn quốc: 25.000đ/đơn (dưới 2kg). Đơn thuê ship ngoài khách tự thanh toán phí ship
Thông tin dược phẩm
Nhà sản xuất:
Số đăng ký:
SP3-1222-21
Hoạt chất:
Bevacizumab 400 mg /16ml
Xuất xứ:
Việt Nam
Dạng bào chế:
Dung dịch tiêm truyền
Đóng gói:
Hộp 1 lọ
Hạn sử dụng:
36 tháng
Video
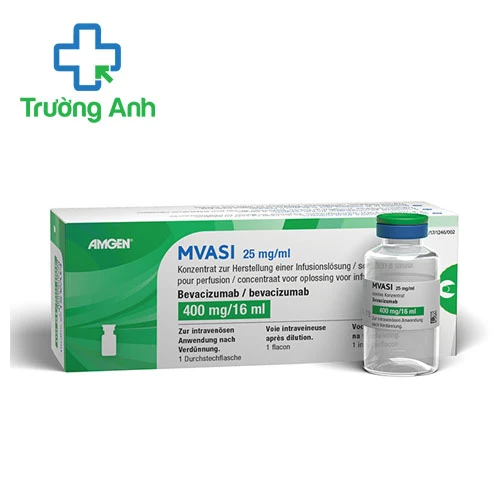
Mvasi 400mg/16ml (Bevacizumab) là gì?
- Mvasi 400mg/16ml (Bevacizumab) là dung dịch tiêm truyền tĩnh mạch với hoạt chất chính Bevacizumab có tác dụng một số loại ung thư như ung thư đại trực tràng di căn, ung thư phổi không tế bào nhỏm u nguyên bào me tái phát, ung thư di căn biểu mô tế bào thận, ung thư cổ tử cung dai dăng…
Thành phần của Mvasi 400mg/16ml (Bevacizumab)
- Bevacizumab: 400mg/16ml.
Dạng bào chế
- Dung dịch tiêm truyền tĩnh mạch.
Ung thư là gì?
- Ung thư là tập hợp các bệnh lý đặc trưng bởi sự phát triển bất thường của các tế bào phân chia không kiểm soát và có khả năng xâm nhập, phá hủy các mô cơ thể bình thường. Hầu hết, các tế bào trong cơ thể có chức năng cụ thể và tuổi thọ cố định..
Công dụng và chỉ định của Mvasi 400mg/16ml (Bevacizumab)
Thuốc Mvasi 400Mg/16Ml có tác dụng trong điều trị bệnh:
- Ung thư đại trực tràng di căn: Thuốc Mvasi (bevacizumab) kết hợp với hóa trị liệu dựa trên fluorouracil tiêm tĩnh mạch, được chỉ định để điều trị bậc một hoặc bậc hai cho bệnh nhân bị ung thư đại trực tràng di căn (mCRC).
Thuốc Mvasi (bevacizumab) kết hợp với hóa trị liệu dựa trên fluoropyrimidine-irinotecan- hoặc fluoropyrimidine-oxaliplatin, được chỉ định để điều trị bậc hai cho những bệnh nhân bị mCRC tiến triển trên phác đồ có sản phẩm bevacizumab bậc một. - Ung thư phổi không tế bào nhỏ dạng không vảy: Thuốc Mvasi (bevacizumab) kết hợp với carboplatin và paclitaxel, được chỉ định để điều trị đầu tay cho những bệnh nhân mắc bệnh ung thư phổi không phải tế bào nhỏ không vảy, tiến triển tại chỗ, tái phát hoặc di căn (NSCLC).
- U nguyên bào men tái phát: Thuốc Mvasi (bevacizumab) được chỉ định để điều trị u nguyên bào thần kinh đệm (GBM) tái phát ở người lớn.
- Ung thư di căn biểu mô tế bào thận: Thuốc Mvasi (bevacizumab) kết hợp với interferon-alfa, được chỉ định để điều trị ung thư biểu mô tế bào thận di căn (mRCC).
- Ung thư cổ tử cung dai dẳng, bị tái phát hoặc di căn: Thuốc Mvasi (bevacizumab) kết hợp với paclitaxel và cisplatin hoặc paclitaxel và topotecan, được chỉ định để điều trị bệnh nhân ung thư cổ tử cung dai dẳng, bị tái phát hoặc di căn.
- Biểu mô buồng trứng, ống dẫn trứng, hoặc ung thư phúc mạc nguyên phát:
- Thuốc Mvasi (bevacizumab) kết hợp với carboplatin và paclitaxel, sau đó là MVASI như một tác nhân duy nhất, được chỉ định để điều trị bệnh nhân ung thư buồng trứng, ống dẫn trứng hoặc phúc mạc giai đoạn III hoặc IV sau khi phẫu thuật cắt bỏ ban đầu.
- Thuốc Mvasi (bevacizumab) kết hợp với paclitaxel, pegylated liposomal doxorubicin, hoặc topotecan, được chỉ định để điều trị cho các bệnh nhân bị ung thư biểu mô buồng trứng, ung thư ống dẫn trứng hoặc bị ung thư phúc mạc tái phát kháng platin đã nhận được không quá 2 phác đồ hóa trị trước đó.
- Thuốc Mvasi (bevacizumab) kết hợp với carboplatin và paclitaxel, hoặc với carboplatin và gemcitabine, sau đó là thuốc Mvasi (bevacizumab) như là một tác nhân duy nhất, và được chỉ định để điều trị bệnh nhân bị tái phát biểu mô nhạy cảm với platin, ung thư ống dẫn trứng, hoặc ung thư phúc mạc nguyên phát.
Cách dùng - Liều dùng của Mvasi 400mg/16ml (Bevacizumab)
- Cách dùng:
- Thuốc dùng đường tiêm truyền.
- Liều dùng:
- Sử dụng thuốc Mvasi 400Mg/16Ml theo chỉ định của bác sĩ điều trị, Liều của thuốc Mvasi 400Mg/16Ml có thể có sự điều chỉnh tùy theo đối tượng cùng thể trạng bệnh của bệnh nhân.
- Ung thư đại trực tràng di căn:
- Liều lượng khuyến cáo khi sử dụng thuốc MVASI kết hợp cùng hóa trị liệu dựa trên fluorouracil tiêm tĩnh mạch là:
- 5 mg / kg tiêm tĩnh mạch khoảng 2 tuần một lần kết hợp với bolus-IFL.
- 10 mg / kg tiêm tĩnh mạch khoảng 2 tuần một lần kết hợp với FOLFOX4.
- 5 mg / kg tiêm tĩnh mạchkhoảng mỗi 2 tuần hoặc 7,5 mg / kg tiêm tĩnh mạch khoảng 3 tuần một lần kết hợp với fluoropyrimidine-irinotecan- hoặc fluoropyrimidine-oxaliplatin hóa trị liệu ở các bệnh nhân tiến triển theo phác đồ đầu tiên có chứa sản phẩm bevacizumab.
- Ung thư phổi không tế bào nhỏ dạng không vảy:Liều khuyến cáo sử dụng 15 mg / kg tiêm tĩnh mạch 3 tuần một lần kết hợp với carboplatin và paclitaxel.
- U nguyên bào men tái phát: Liều khuyến cáo sử dụng 10 mg / kg tiêm tĩnh mạch 2 tuần một lần.
- Ung thư di căn biểu mô tế bào thận: Liều khuyến cáo sử dụng 10 mg / kg tiêm tĩnh mạch khoảng 2 tuần một lần kết hợp với interferon-alfa.
- Ung thư cổ tử cung dai dẳng, tái phát hoặc di căn: Liều khuyến cáo là 15 mg / kg tiêm tĩnh mạch khoảng 3 tuần một lần kết hợp với paclitaxel và cisplatin, hoặc là kết hợp với paclitaxel và topotecan.
- Biểu mô buồng trứng, ống dẫn trứng, hoặc ung thư phúc mạc nguyên phát:
- Bệnh tại giai đoạn III hoặc IV sau khi phẫu thuật cắt bỏ ban đầu
Liều khuyến cáo là 15 mg / kg tiêm tĩnh mạch khoảng 3 tuần một lần kết hợp cùng carboplatin và paclitaxel trong tối đa 6 chu kỳ, tiếp theo là MVASI 15 mg / kg khoảng mỗi 3 tuần như là một tác nhân duy nhất trong tổng số lên đến 22 chu kỳ hoặc là cho đến khi bệnh tiến triển. , tùy thuộc điều kiện nào xảy ra sớm hơn. - Bệnh tái phát
- Kháng bạch kim:
- Liều khuyến cáo sử dụng 10 mg / kg tiêm tĩnh mạch khoảng 2 tuần một lần kết hợp với paclitaxel, hoặc pegylated liposomal doxorubicin, hoặc topotecan (mỗi tuần).
- Liều khuyến cáo sử dụng 15 mg / kg tiêm tĩnh mạch khoảng 3 tuần một lần kết hợp với topotecan (3 tuần một lần).
- Bạch kim nhạy cảm:
- Liều khuyến cáo sử dụng 15 mg / kg tiêm tĩnh mạch 3 tuần một lần, kết hợp cùng carboplatin và paclitaxel trong 6 đến 8 chu kỳ, sau đó là thuốc MVASI 15 mg / kg khoảng 3 tuần như một tác nhân duy nhất cho tới khi bệnh tiến triển.
- Liều khuyến cáo là 15 mg / kg tiêm tĩnh mạch khoảng 3 tuần một lần, kết hợp cùng carboplatin và gemcitabine trong 6 đến 10 chu kỳ, tiếp theo là thuốc MVASI 15 mg / kg mỗi 3 tuần như một tác nhân duy nhất cho đến khi bệnh tiến triển.
- Bệnh tại giai đoạn III hoặc IV sau khi phẫu thuật cắt bỏ ban đầu
Chống chỉ định của Mvasi 400mg/16ml (Bevacizumab)
- Không dùng cho người mẫn cảm với bất kỳ thành phần nào của thuốc.
Lưu ý khi sử dụng Mvasi 400mg/16ml (Bevacizumab)
- Các lỗ thủng và lỗ rò đường tiêu hóa: Thủng đường tiêu hóa nghiêm trọng, và đôi khi gây tử vong xảy ra với tỷ lệ cao hơn ở bệnh nhân dùng sản phẩm bevacizumab so với bệnh nhân được hóa trị. Phần lớn các lỗ thủng xảy ra trong vòng 50 ngày kể từ ngày dùng liều đầu tiên
- Các biến chứng phẫu thuật và chữa lành vết thương: Trong một nghiên cứu lâm sàng có kiểm soát, trong đó bevacizumab không được sử dụng trong vòng 28 ngày sau những thủ thuật phẫu thuật lớn, tỷ lệ biến chứng lành vết thương, bao gồm những biến chứng nghiêm trọng và tử vong, là 15% ở bệnh nhân mCRC đã trải qua phẫu thuật trong khi dùng bevacizumab và 4% ở bệnh nhân người không nhận được bevacizumab. Trong một nghiên cứu lâm sàng có đối chứng ở những bệnh nhân bị GBM tái phát hoặc tái phát, tỷ lệ biến cố lành vết thương là 5% ở những bệnh nhân đã dùng bevacizumab và 0,7% ở những bệnh nhân không dùng bevacizumab.
- Xuất huyết: Các sản phẩm của Bevacizumab có thể gây ra hai dạng chảy máu riêng biệt: xuất huyết nhẹ, thường là chảy máu cam cấp độ 1 và xuất huyết nghiêm trọng, trong một số trường hợp đã gây tử vong. Xuất huyết nghiêm trọng hoặc gây tử vong, bao gồm ho ra máu, xuất huyết tiêu hóa, nôn trớ, xuất huyết thần kinh trung ương, chảy máu cam và chảy máu âm đạo thường xuyên hơn gấp 5 lần ở bệnh nhân sử dụng bevacizumab so với bệnh nhân chỉ hóa trị. Trong các nghiên cứu lâm sàng, tỷ lệ các biến cố xuất huyết Mức độ 3-5 dao động từ 0,4% đến 7% ở bệnh nhân dùng bevacizumab
- Sự kiện huyết khối động mạch: Các biến cố huyết khối động mạch (ATE) nghiêm trọng, đôi khi gây tử vong, bao gồm nhồi máu não, cơn thoáng thiếu máu cục bộ, nhồi máu cơ tim và đau thắt ngực xảy ra với tỷ lệ cao hơn ở bệnh nhân dùng bevacizumab so với bệnh nhân được hóa trị. Trong các nghiên cứu lâm sàng, tỷ lệ ATE Cấp độ 3-5 là 5% ở bệnh nhân dùng bevacizumab với hóa trị liệu so với ≤ 2% ở bệnh nhân chỉ hóa trị liệu; tỷ lệ cao nhất xảy ra ở bệnh nhân GBM. Nguy cơ phát triển ATE tăng lên ở những bệnh nhân có tiền sử huyết khối động mạch, tiểu đường hoặc> 65 tuổi
- Sự kiện huyết khối tĩnh mạch: Tăng nguy cơ biến cố huyết khối tĩnh mạch (VTE) đã được quan sát thấy trong các nghiên cứu lâm sàng
- Tăng huyết áp: Tăng huyết áp nghiêm trọng xảy ra với tỷ lệ cao hơn ở những bệnh nhân dùng các sản phẩm bevacizumab so với những bệnh nhân được hóa trị liệu một mình. Trong các nghiên cứu lâm sàng, tỷ lệ tăng huyết áp Độ 3-4 dao động từ 5% đến 18%. Theo dõi huyết áp hai đến ba tuần một lần trong khi điều trị bằng MVASI. Điều trị bằng liệu pháp chống tăng huyết áp thích hợp và theo dõi huyết áp thường xuyên. Tiếp tục theo dõi huyết áp đều đặn ở những bệnh nhân bị tăng huyết áp do MVASI gây ra hoặc-cơn kịch phát sau khi ngừng MVASI. Giữ lại MVASI ở bệnh nhân tăng huyết áp nặng mà không được kiểm soát bằng quản lý y tế; tiếp tục sau khi được kiểm soát với quản lý y tế. Ngừng điều trị ở những bệnh nhân phát triển cơn tăng huyết áp hoặc bệnh não do tăng huyết áp.
- Hội chứng bệnh não có thể đảo ngược sau: Hội chứng bệnh não có hồi phục sau (PRES) được báo cáo ở <0,5% bệnh nhân trong các nghiên cứu lâm sàng. Sự khởi đầu của các triệu chứng xảy ra từ 16 giờ đến 1 năm sau liều đầu tiên. PRES là một rối loạn thần kinh có thể biểu hiện với đau đầu, hôn mê, lú lẫn, co giật, mù và những rối loạn thị giác và thần kinh khác. Có thể có tăng huyết áp từ nhẹ đến nặng.
Sử dụng cho phụ nữ có thai hoặc đang cho con bú
- Phụ nữ có thai hoặc đang cho con bú tham khảo ý kiến bác sĩ
Sử dụng cho người lái xe và vận hành máy móc
- Người lái xe và vận hành máy móc tham khảo ý kiến bác sĩ.
Tác dụng phụ của thuốc Mvasi 400mg/16ml (Bevacizumab)
- Phổ biến hơn: đầy hơi, chảy máu cam, thay đổi khẩu vị hoặc mùi khác thường hoặc khó chịu (sau), thay đổi cách đi lại và thăng bằng, vụng về hoặc không vững, khô miệng, chảy nhiều nước mắt, rụng tóc, đau bụng, tóc mỏng, giảm cân
- Các tác dụng phụ cần phải được chăm sóc y tế ngay lập tức
- Gọi ngay cho bác sĩ của bạn ngay lập tức nếu bạn có bất kỳ tác dụng phụ nào sau đây khi dùng bevacizumab như
- Các tác dụng phụ thường gặp là Ngứa ran, Nóng rát, tê hoặc đau ở bàn tay, cánh tay, bàn chân hoặc chân, Xi măng đen, Chảy máu nướu răng, Đau nhức cơ thể, Đau hoặc khó chịu ở ngực, Ớn lạnh, Nước tiểu có mây, Ho, Vết nứt trên da, Giảm lượng nước tiểu, Khó chịu hụt hơi hoặc khó thở, Giãn tĩnh mạch cổ, ngất xỉu hoặc choáng váng khi bạn đứng lên, đột ngột từ tư thế nằm hoặc ngồi, Nghẹt tai, Mệt mỏi hoặc suy nhược cực độ, Sốt, Thở không đều, Nhịp tim không đều, Thiếu hoặc mất sức lực, Chóng mặt, Chán ăn, Mất sức, cơ thể nóng, Mất giọng, Thay đổi tâm trạng, Nghẹt mũi, Lo lắng, đỏ hoặc sưng ở tay hoặc chân, Đi tiểu đau hoặc khó khăn, Xác định các nốt đỏ trên da, Nhói thình thịch trong tai, Thở nhanh, Đỏ mặt, Chảy nước mũi, Co giật, Kim và kim châm vào cảm giác, Vết loét trên da, vết loét hoặc đốm trắng trên môi hoặc trong miệng, Đau nhói, Mắt trũng , Khối u, Đổ mồ hôi, Sưng mặt, ngón tay, bàn chân hoặc chân, Sưng hoặc viêm miệng, Viêm tuyến, Khát nước, Nôn ra máu hoặc chất giống bã cà phê, Chảy nước hoặc có máu tiêu chảy, Tăng cân, Da nhăn nheo, Da vàng…
- Các tác dụng phụ ít gặp như Đau nhức xương, Khó nuốt, Ngất xỉu, Táo bón nặng, Nôn nhiều, Đau dạ dày hoặc đau, Hiếm gặp, Đau lưng, Chảy máu, Nhìn mờ, Lú lẫn, Chóng mặt, Buồn ngủ, Nhức đầu, Tấn công, tăng khát dần dần, Mất ý thức, Đau cơ hoặc chuột rút, Vết loét, Da nhợt nhạt
- Tỷ lệ mắc chưa biết: Chất nhầy có máu hoặc chảy máu cam không rõ nguyên nhân, Táo bón, Tiêu chảy, Ợ chua, Nặng hàm, Sốt cao, Khàn giọng, Khó tiêu, Rung răng lung lay, Buồn nôn, Đau, sưng hoặc tê ở miệng hoặc hàm, Đau bụng dữ dội, Bụng đau hoặc nóng rát, Đau dạ dày, thường sau khi ăn xong, Yếu, đột ngột đau cánh tay hoặc chân Đau đột ngột, dữ dội ở ngực, Chảy máu hoặc bầm tím không rõ nguyên nhân, Mệt mỏi hoặc suy nhược bất thường, Thay đổi giọng nói…
- Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng.
Tương tác
- Thuốc Mvasi 400mg/16ml có thể tương tác với một số loại thuốc như: Adriamycin (doxorubicin), Alphanate (antihemophilic factor / von willebrand factor), amlodipine, aspirin, Banzel (rufinamide), BayGam (immu globulin tiêm bắp), Benadryl (diphenhydramine), bleomycin , Cafergot (caffeine / ergotamine), ceftriaxone, chloramphenicol, clonidine, Clozaril (clozapine), Complera (emtricitabine / rilpivirine, tenofovir), Corlanor (ivabradine), lisinolatepril, Lomotil (atropine / diphenoxylate / lướt sóng) trifluridine), Ritalin (methylphenidate), Xanax (alprazolam)
Quên liều và cách xử trí
- Dùng liều đó ngay khi nhớ ra. Không dùng liều thứ hai để bù cho liều mà bạn có thể đã bỏ lỡ. Chỉ cần tiếp tục với liều tiếp theo.
Quá liều và cách xử trí
- Nếu quá liều xảy ra cần báo ngay cho bác sĩ, hoặc thấy có biểu hiện bất thường cần tới bệnh viện để được điều trị kịp thời.
Bảo quản
- Bảo quản ở nhiệt độ thoáng mát dưới 30 độ c.
- Để xa tầm tay trẻ em.
Quy cách đóng gói
- Hộp 1 lọ.
Nhà sản xuất
- Amgen – Mỹ.
Sản phẩm tương tự
Câu hỏi thường gặp
Tuyên bố miễn trừ trách nhiệm:
Mục tiêu của chúng tôi là cung cấp cho bạn thông tin hiện tại và phù hợp nhất. Tuy nhiên, vì thuốc tương tác khác nhau ở mỗi người, chúng tôi không thể đảm bảo rằng thông tin này bao gồm tất cả các tương tác có thể. Thông tin này không thay thế cho lời khuyên y tế. Luôn luôn nói chuyện với nhà cung cấp dịch vụ chăm sóc sức khỏe của bạn về các tương tác có thể xảy ra với tất cả các loại thuốc theo toa, vitamin, thảo dược và chất bổ sung, và các loại thuốc không kê đơn mà bạn đang dùng.
Sản phẩm liên quan
Sản phẩm cùng hãng
Bình luận
Bạn hãy là người đầu tiên nhận xét về sản phẩm này